Пресс-центр / новости / Наука /
Основные научные достижения Института в 2012 году
21 декабря 2012 г. в Институте состоялось заседание Ученого совета, на котором были рассмотрены итоги выполнения НИР в уходящем году. Ниже приведены краткие аннотации научных достижений, представленные руководителями подразделений (все материалы приведены в авторской редакции).
Оглавление: Лаборатория биомолекулярной ЯМР спектроскопии — Лаборатория углеводов — Лаборатория моделирования биомолекулярных систем — Лаборатории молекулярных технологий и биофотоники — Лаборатория рентгеноструктурного анализа — Отдел молекулярных основ нейросигнализации — Лаборатория механизмов генной экспрессии — Лаборатории протеомики и химии пептидов — Лаборатория молекулярной иммунологии — Отдел биоинженерии — Лаборатория сравнительной и функциональной геномики — Лаборатория молекулярной биофизики — Лаборатория геномики адаптивного иммунитета — Лаборатория биокатализа — Лаборатория протеомики — Лаборатория нейрорецепторов и нейрорегуляторов — Лаборатория клеточных взаимодействий — Лаборатория структуры и функций генов человека — Группа кросс-сшивающих ферментов
I. Фундаментальные исследования биообъектов
Лаборатория биомолекулярной ЯМР спектроскопии — Молекулярные механизмы патогенеза болезни Альцгеймера
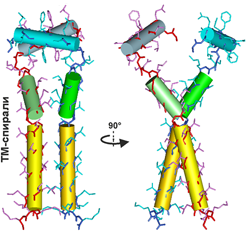
Исследование пространственной структуры и внутримолекулярной динамики ТМ-доменов белка-предшественника β-амилоида APP, ассоциированного с развитием болезни Альцгеймера.
Проведены исследования структурно-динамических процессов, происходящих при димеризации трансмембранных (ТМ) доменов битопных мембранных белков в липидном окружении на примере ТМ-домена белка-предшественника β-амилоида APP, ассоциированного с развитием болезни Альцгеймера. Для гомодимерных ТМ-доменов APP получены структурно-динамические данные о димеризации ТМ-доменов, солюбилизированных в детергентных мицеллах
ТМ-α-спираль APPtm Lys699—Lys724 димеризуется по длинному гептадному мотиву I702X3M706X2G709X3A713X2I716X3I720X2I723, в то время как примембранный участок находится в равновесии между α-спиральной конформацией и неупорядоченным клубком. Под петлевым участком в области контакта JM-спирали с поверхностью мембраны рядом с N-концом ТМ-спирали, по-видимому, образуется гидрофобная полость, предназначенная для взаимодействия APP с холестерином. Важно отметить, что семейные мутации, ассоциированные с ранним развитием болезни Альцгеймера, сосредоточены как рядом с ТМ-сайтами расщепления APP γ-секретазой, так и на С-конце JM-спирали, где расположены ионогенные остатки Asp693 и Glu694.
- E.V. Bocharov, K.V. Pavlov, P.E. Volynsky, R.G. Efremov, A.S. Arseniev. (2012). Structure-Functional Insight Into Transmembrane Helix Dimerization. Protein Engineering 2012,
1–32, ISBN: 978-953-51-0037-9; - K.D. Nadezhdin, O.V. Bocharova, E.V. Bocharov, A.S. Arseniev. (2012). Dimeric Structure of Transmembrane Domain of Amyloid Precursor Protein in Micellar Environment. FEBS Lett. 586,
1687–1692.
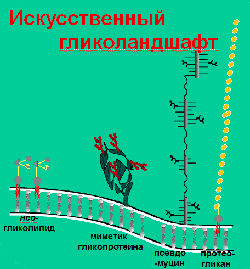
Лаборатория углеводов — Искусственный гликоландшафт
Синтезирована большая группа липофильных молекул, которую можно назвать «тулбокс» для исследования процессов в гликокаликсе. Липофильные гликаны и пептиды способны в мягких условиях встраиваться в мембрану живой клетки.
Для этого были использованы два липофильных якоря: холестерил и остаток диолеоилфосфатидилэтаноламина (ДОФЭ). Эти молекулы быстро и контролировано встраиваются в клетку, и довольно долго в ней остаются. Два типа якорей и несколько типов спейсеров разной длины (до 15 нм) позволяют проводить встраивание равномерно, кластерно и адресуя лиганд на нужный «этаж» гликокаликса. Синтезирован также вариант с тремя жесткими антеннами, расстояние между привязанными к концам которых лигандами точно задано благодаря жесткости конструкции.
Показано, что все эти конструкции функциональны, то есть, будучи встроенными в клеточную мембрану, способны связываться с соответствующим лектином или антителом.
Лаборатория моделирования биомолекулярных систем — Моделирование пространственной структуры и динамики олигомеров трансмембранных α-спиралей в белках
Пространственная организация и функционирование трансмембранных (ТМ) димеров и олигомеров белковых α-спиралей играют важную роль в передаче сигналов через биологическую мембрану и обусловливает множество биологических событий, таких как рост и слияние клеток, а также патогенез многих заболеваний (см. Достижение лаборатории ЯМР). В Лаборатории ЛМБС разработан оригинальный вычислительный подход, позволяющий предсказывать возможное строение ТМ-димеров и олигомеров белковых спиралей на основе их аминокислотной последовательности и детальных моделей липидных бислоев, в которых рассчитывается молекулярная динамика (МД) этих систем.
Созданный алгоритм предсказания возможной структуры димера (PREDDIMER) основан на сопоставлении цилиндрических «разверток» (карт) гидрофобных / гидрофильных свойств и рельефа индивидуальных α-спиралей в составе ди- или олигомера, а полноатомное моделирование МД в составе липидного бислоя позволяет достичь оптимизации предсказанной «стартовой» геометрии с учетом физико-химических свойств конкретного выбранного липидного бислоя, а также рассчитать свободную энергию образования комплекса в этой сложной супрамолекулярной системе.
Одним из важных результатов разработки этого комплексного алгоритма стало понимание того, что строение димера определяется не только (а иногда даже и не столько) параметрами ТМ-сегментов белка, но свойствами липида, составляющего бислой (важна, например, толщина гидрофобного слоя, насыщенность ацильных цепей и т.д.).
- Polyansky A.A., Volynsky P.E., Efremov R.G. (2012). Multistate organization of transmembrane helical protein dimers governed by the host membrane. J. Amer. Chem. Soc. 134,
14390–14400; - Полянский А.А., Чугунов А.О., Волынский П.Е., Ефремов Р.Г. Свидетельство о государственной регистрации программы для ЭВМ № 2012618494 от 19.09.2012 г., «PREDDIMER», патентообладатель: ИБХ РАН.
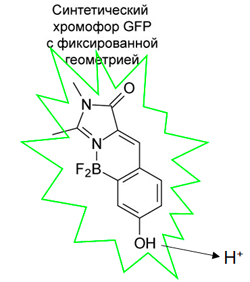
Лаборатории молекулярных технологий и биофотоники — Синтетический аналог хромофора GFP с высоким квантовым выходом флуоресценции и эффективным переносом протона в возбужденном состоянии
Впервые синтезирован близкий аналог хромофора GFP с жестко фиксированной конформационной подвижностью (отсутствием возможности цис—транс изомеризации). Для этого использовалась недавно открытая реакция борирования биарильных соединений, содержащих атом азота в орто-положении одного из ароматических колец. Полученный синтетический хромофор HBDI-BF2 обладал яркой флуоресценцией с квантовым выходом, достигающим 0.73 (в ацетонитриле), сходным с аналогичным значением для GFP (0.79). При этом максимумы поглощения и испускания этого соединения были близки к аналогичным параметрам GFP и его хромофора и имели лишь небольшой батохромный сдвиг.
Уникальной особенностью хромофора HBDI-BF2 является его способность к переносу протона в возбужденном состоянии (excited-state proton transfer, ESPT). Данный эффект хорошо изучен для белка GFP дикого типа медузы Aequorea victoria и некоторых других флуоресцентных белков и сенсоров, однако до сих пор его не удавалось наблюдать на синтетических аналогах хромофора GFP. Таким образом, хромофор HBDI-BF2 является прекрасной моделью для изучения флуоресценции и ESPT хромофоров флуоресцентных белков вне белкового окружения.
Следует также отметить, что полученные данные о свойствах HBDI-BF2, а именно, высокий квантовый выход, наличие полос поглощения и флуоресценции в видимой области спектра, а также высокая растворимость в воде и небольшой размер молекулы свидетельствуют о перспективности использования подобных соединений в роли флуоресцентных красителей для мечения в биологических системах.
- Baranov M.S., Lukyanov K.A., Borissova A.O., Shamir J., Kosenkov D., Slipchenko L.V., Tolbert L.M., Yampolsky I.V., Solntsev K.M. (2012). Conformationally locked chromophores as models of excited-state proton transfer in fluorescent proteins. J. Am. Chem. Soc. 134,
6025–6032.
Лаборатория рентгеноструктурного анализа — Супердальнекрасные флуоресцентные белки
Флуоресцентные белки (ФБ) с эмиссией в красной и особенно в дальнекрасной областях спектра представляют особый практический интерес для целей визуализации биологических процессов в живых организмах в связи с повышенной прозрачностью биологических тканей для соответствующего излучения.
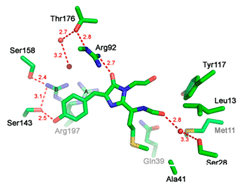
В 2012 году методом рентгеноструктурного анализа установлены пространственные структуры супердальнекрасных ФБ eqFP650 (lex/lem: 592/650 нм) и eqFP670 (lex/lem: 605/670 нм), генно-инженерных вариантов дальнекрасного ФБ Katushka (lex/lem: 588/635 нм) (при разрешении 1.8 и 1.6 Å, соответственно). Методом сайт-направленного мутагенеза детально изучена взаимосвязь между пространственной организацией и фотофизическими характеристиками (получены и исследованы фотофизические характеристики восьми генно-инженерных вариантов).
Анализ полученных структур выявил две группы важных структурных изменений, ответственных за батохромный («красный») сдвиг полос возбуждения/эмиссии у этих биомаркеров относительно предшественника Katushka. Показано, что первая группа изменений приводит к увеличению гидрофильности со стороны ацилиминной связи хромофора за счет появления одной и трех молекул воды в структурах eqFP650 и eqFP670, соответственно. Вторая группа изменений, установленная только для eqFP670, связана с заменами остатков Ser143 и Ser158, располагающихся в предшественнике Katushka со стороны p-оксифенильной группы хромофора, на остаток Asn.
Координаты атомов двух новых кристаллических структур eqFP650 и eqFP670 были депонированы в Международный структурный банк белков с кодами доступа 4EDO и 4EDS, соответственно.
Отдел молекулярных основ нейросигнализации — Новый класс пептидных токсинов — блокаторов никотиновых холинорецепторов
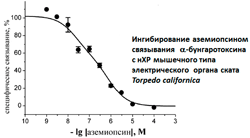
При проведении протеомных исследований змеиных ядов открыт новый блокатор никотиновых холинорецепторов (нХР) — пептид аземиопсин из яда гадюки Azemiops feae [1]. Все известные до сих пор природные токсины, способные взаимодействовать с нХР содержат от двух (a-конотоксины) до пяти (a-нейротоксины змей) дисульфидных связей. Наличие дисульфидов абсолютно необходимо для сохранения биологической активности этих токсинов. В отличие от них, аземиопсин вообще не содержит дисульфидных связей, что упрощает конструирование и синтез на его основе новых соединений с миорелаксантной активностью [2]. Тем самым открываются новые возможности для направленного воздействия на биологически важные системы, в функционировании которых участвуют нХР.
- Utkin Y.N., Weise C., Kasheverov I.E., Andreeva T.V., Kryukova E.V., Zhmak M.N., Starkov V.G., Hoang N.A., Bertrand D., Ramerstorfer J., Sieghart W., Thompson A.J., Lummis S.C., Tsetlin V.I. (2012). Azemiopsin from Azemiops feae viper venom, a novel polypeptide ligand of nicotinic acetylcholine receptor. J. Biol. Chem. 287,
27079–27086. - Уткин Ю.Н., Андреева Т.В., Вайзе К., Старков В.Г., Жмак М.Н., Кашеверов И.Е., Цетлин В.И. Пептид аземиопсин, избирательно взаимодействующий с никотиновыми холинорецепторами мышечного типа и пригодный для использования в качестве мышечного релаксанта в медицине и косметологии. Заявка на патент РФ № 2011143065 от 26.10.2011. Решение о выдаче патента от 10.06.2012.
Лаборатория механизмов генной экспрессии — Белки-партнёры изоформ hRPB11ba и hRPB11ca субъединицы РНК-полимеразы II человека POLR2J (hRPB11)
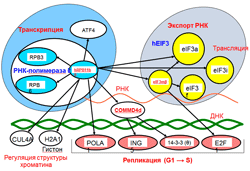
Определены спектры белковых партнёров новых изоформ hRPB11ba и hRPB11сa субъединицы РНК-полимеразы II человека POLR2J в нервной (эмбриональный мозг) и лимфоидной (клеточная линия Jurkat) тканях Homo sapiens. Функциональные характеристики обнаруженных белков-партнёров hRPB11ba и hRPB11сa в протеомах как нервной, так и иммунной тканей человека указывают на то, что эти изоформы, подобно основной (мажорной) субъединице РНК-полимеразы II hRPB11a, являются компонентами (субъединицами особых форм РНК-полимеразы II) определённых транскрипционных комплексов и участвуют не только в транскрипции некоторых ДНК-матриц, но и вовлечены в более поздние стадии биогенеза мРНК (процессинг, транспорт из ядра к транслирующим полисомам). Впервые определены белки, взаимодействующие in vivo с обнаруженными нами ранее новыми компонентами протеома человека eIF3mb и COMMD4d — важными партнёрами минорных субъединиц РНК-полимеразы II человека hRPB11ba и hRPB11ca. Таковыми оказались, прежде всего, важнейшие регуляторы клеточного цикла на стадии перехода G1→S транскрипционный фактор E2F1, активатор тирозиновых и триптофановых монооксигеназ 14-3-3 и онкосупрессор II типа ING5, а также ряд белков шапероновых комплексов, прежде всего TRiC (TCP1 ring complex), среди которых шаперонин CCT4 (SRB) взаимодействует с обоими белками (и с COMMD4d, и с eIF3mb). Обнаруженные взаимодействия указывают на существование особых путей сопряжения процессов репликации и транскрипции в ядрах клеток человека.
- Шематорова Е.К., Шпаковский Д.Г., Шпаковский Г.В. (2013). Новые комплексы генной экспрессии и их роль в возникновении и эволюции рода Homo. Цитология 55, принята в печать 07.12.2012.
- Прошкин С.А., Шематорова Е.К., Суслова Е.А., Прошкина Г.М., Шпаковский Г.В. (2011). Минорная изоформа субъединицы РНК-полимеразы II человека hRPB11 (POLR2J) взаимодействует с несколькими субъединицами фактора инициации трансляции eIF3. Биохимия 76,
1195–1200.
II. Методические достижения и успехи в нанобиоинженерии
Лаборатории протеомики и химии пептидов — Системный анализ пептидома, протеома и транскриптома мха Physcomitrella patens
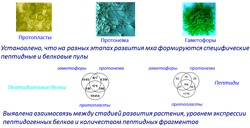
Установлено, что на разных этапах развития мха формируются специфические пептидные и белковые пулы. Выявлена взаимосвязь между стадией развития растения, уровнем экспрессии пептидогенных белков и количеством пептидных фрагментов.
Лаборатория молекулярной иммунологии — Разработка фундаментальных принципов конструирования неприродных антител с заданными свойствами и нанокомплексов на их основе
Впервые на универсальной платформе белкового модуля барназа—барстар создан и охарактеризован целый ряд самоассоциирующихся надмолекулярных комплексов, состоящих из противоопухолевых мини-антител различной специфичности и флуоресцентных полупроводниковых нанокристаллов (квантовых точек) с разным спектром флуоресценции [1, 2]. С использованием созданных надмолекулярных комплексов получены прижизненные изображения аденокарциномы молочной железы человека, привитой иммунодефицитным мышам. Показано, что такое специфическое мечение опухоли позволяет получить более контрастное изображение, а также увеличить интенсивность и длительность сигнала в
- Zdobnova T.A., Stremovskiy O.A., Lebedenko E.N., Deyev S.M. (2012). Self-assembling complexes of quantum dots and scFv antibodies for cancer cell targeting and imaging. PLoS One 7, e48248;
- Balalaeva I.V., Zdobnova T.A., Krutova I.V., Brilkina A.A., Lebedenko E.N., Deyev S.M. (2012). Passive and active targeting of quantum dots for whole-body fluorescence imaging of breast cancer xenografts. J. Biophotonics 5,
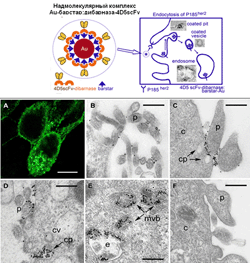
860–867; - Ivanova J.L., Edelweiss E.F., Leonova O.G., Balandin T.G., Popenko V.I., Deyev S.M. (2012). Application of fusion protein 4D5 scFv—dibarnase:barstar—gold complex for studying P185HER2 receptor distribution in human cancer cells. Biochimie 94,
1833–1836.
Отдел биоинженерии — Новая холодоактивная эстераза Грам-отрицательной бактерии Psychrobacter cryohalolentis, выделенной из вечной мерзлоты
В результате анализа генома бактерии Psychrobacter cryohalolentis, выделенной из вечной мерзлоты, обнаружены кодирующие последовательности липолитических ферментов. Клонирован ген одного из них — эстеразы P. cryohalolentis (EstPc) — и сконструирован высокоэффективный штамм-продуцент фермента. Исследование EstPc показало, что он обладает рядом уникальных свойств — в частности, проявляет максимальную активность при 35 °С, при этом его активность в диапазоне
- Петровская Л.Е., Новотоцкая-Власова К.А., Спирина Е.В., Хохлова Г.В., Ривкина Е.М., Гиличинский Д.А., Долгих Д.А., Кирпичников М.П. (2012). Липолитические ферменты микроорганизмов из криопэгов вечной мерзлоты. Доклады Академии Наук 445,
102–105. - Novototskaya-Vlasova K., Petrovskaya L., Yakimov S., Gilichinsky D. (2012). Cloning, Purification, and Characterization of a Cold-Adapted Esterase Produced by Psychrobacter cryohalolentis K5(T) from Siberian Cryopeg. FEMS Microbiology Ecology 82,
367–375.
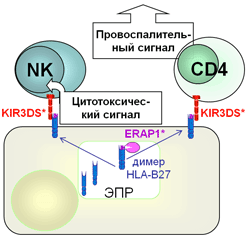
Лаборатория сравнительной и функциональной геномики — Мультилокусный ассоциативный анализ и предрасположенность к развитию анкилозирующего спондилита у населения европейской части России
Мультилокусный анализ — современный биоинформатический подход к комплексной идентификации генетической предрасположенности — обладает повышенной прогностической ценностью, поскольку позволяет количественно определять совместный вклад в развитие признака многих структурно несвязанных генов. Специализированное программное обеспечение отечественной разработки (ПО APSampler) использовано нами для мультилокусного анализа генетических факторов предрасположенности к развитию анкилозирующего спондилита (АС) — аутоиммунного заболевания с хроническим воспалением суставов осевого скелета. Исследование проведено на адекватных, уравновешенных по половому и возрастному составу выборках из городского населения центрального региона России. В обе выборки — здоровых доноров и больных АС — включены исключительно носители ассоциированного с заболеванием аллеля HLA-B27. Предварительное генотипирование обеих выборок проводили по 9 функционально значимым маркерам трех несцепленных кандидатных генов: KIR3D, MICA и ERAP1. Сравнительный мультилокусный анализ генотипов двух выборок выявил наличие двух аллельных сочетаний, достоверно преобладающих у больных и представляющих выраженный генетический риск (OR>4.2) развития заболевания. Полученные данные и их анализ существенно расширяют современные представления об этиологии анкилозирующего спондилита. Набор молекулярно-генетических маркеров, сконструированный для выявленных аллельных сочетаний, может быть использован при расширенной диагностике и прогнозировании развития данного аутоиммунного заболевания.
- Bolotin D.A., Mamedov I.Z., Britanova O.V., Zvyagin I.V., Shagin D., Ustyugova S.V., Turchaninova M.A., Lukyanov S., Lebedev Y.B., Chudakov D.M. (2012). Next generation sequencing for TCR repertoire profiling: platform-specific features and correction algorithms. Eur. J. Immunol. 42,
3073–3083; - Britanova O.V., Bochkova A.G., Staroverov D.B., Fedorenko D.A., Bolotin D.A., Mamedov I.Z., Turchaninova M.A., Putintseva E.V., Kotlobay A.A., Lukyanov S., Novik A.A., Lebedev Y.B., Chudakov D.M. (2012). First autologous hematopoietic SCT for ankylosing spondylitis: a case report and clues to understanding the therapy. Bone Marrow Transplant. 47,
1479–1481.
Лаборатория молекулярной биофизики — Флуоресцентные нанозонды на основе конъюгатов sdAbs—QD (однодоменных антител и квантовых точек)
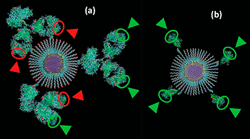
Совместно с французскими учеными разработан новый тип нанозондов на основе конъюгатов однодоменных антител и квантовых точек в форме коллоидных нанокристаллов. Размер предлагаемых нанозондов существенно меньше размера нанозондов на основе полноразмерных антител, что открывает новые возможности при мечении биологических объектов за счет повышения степени проникновения таких нанозондов в ткани и клетки, а также за счет использования сайтов мишеней, недоступных для полноразмерных антител.
Общая стратегия мечения и формирования флуоресцентных нанозондов на основе квантовых точек (КТ) основана на использовании полноразмерных моноклональных антител (mAbs).Недостатком подхода является сравнительно большой размер mAbs. Кроме того, конъюгирование часто приводит к нарушению структуры mAb и формированию нанозондов с неконтролируемой ориентацией mAbs на поверхности КТ. Предлагаемый подход позволяет обойти эти недостатки путем использования однодоменных миниантител (sdAbs), производимых в организме верблюдовых (лама). Мономерные sdAbs в 10 раз меньше mAbs, стойки при экстремальных значениях рН и к агрессивным химическим агентам, стойки к протеолизу и к денатурации при высоких температурах (до 80 °C) и демонстрируют превосходную способность к восстановлению вторичной структуры (рефолдинг). В предлагаемых нанозондах для связывания sdAbs с квантовыми точками вводили дополнительный остаток цистеина в области
Возможности нанозондов продемонстрированы на примере анализа селективности и эффективности мечения линии раковых клеток MC38 и МС38-СЕА, активно экспрессирующих СЕА-антиген. Показано, что чувствительность выявления CEA методом проточной цитометрии существенно увеличена за счет использования sdAbs—КТ нанозондов. Показано, что sdAbs—КТ стабильны и сохраняют специфичность CEA-экспрессирующим опухолевым клеткам в сыворотке крови человека. Продемонстрированы возможности использования sdAbs—КТ нанозондов для иммуногистохимического мечения клинических биопсийных тканей.
Размер формируемых частиц существенно уменьшен по сравнению с нанозондами на основе полноразмерных антител (с 35 нм до 12 нм), что открывает новые возможности при мечении биологических объектов за счет повышения степени проникновения таких нанозондов в ткани и клетки, а также за счет использования сайтов мишеней, недоступных для полноразмерных антител.
- Sukhanova A., Even-Desrumeaux K., Millot J.-M., Chames P., Baty D., Artemyev M., Oleinikov V., Cohen J.H.M., Nabiev I. (2012). Oriented conjugates of monoclonal and single-domain antibodies with quantum dots for flow cytometry and immunohistochemistry diagnostic applications. Proc. of SPIE 8232, 82320T;
- Sukhanova A., Even-Desrumeaux K., Kisserli A., Tabary T., Reveil B., Millot J.M., Chames P., Baty D., Artemyev M., Oleinikov V., Pluot M., Cohen J.H., Nabiev I. (2012). Oriented conjugates of single-domain antibodies and quantum dots: toward a new generation of ultrasmall diagnostic nanoprobes. Nanomedicine 8,
516–525; - Sukhanova A., Even-Desrumeaux K., Chames P., Baty D., Artemyev M., Oleinikov V., Nabiev I. (2012). Engineering of ultra-small diagnostic nanoprobes through oriented conjugation of single-domain antibodies and quantum dots. Prot. exchange.
Лаборатория геномики адаптивного иммунитета — Молекулярное баркодирование, технологии анализа репертуаров Т-клеточных рецепторов
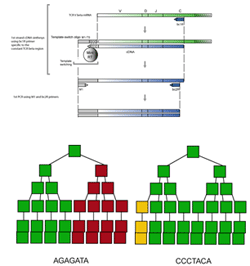
Отработана технология встраивания молекулярных баркодов на уровне синтеза кДНК библиотек генов Т-клеточных рецепторов и антител, при которой уникальный молекулярный баркод, маркирующий каждое событие обратной транскрипции, содержится непосредственно в адаптере для создания универсального сайта отжига праймера на 5’-конце библиотеки по технологии «смены матрицы», с последующим удалением из реакции дезокси-урацил-содержащего 5’-адаптера с использованием фермента UDG.
Получены первые данные по анализу репертуаров Т-клеточных рецепторов с применением молекулярного баркодирования. Показано, что применение молекулярного баркодирования позволяет очень четко нормировать библиотеки, повышает точность анализа разнообразия репертуаров ТКР и соответственно качество сравнительного анализа данных для разных образцов и пациентов.
Разработано соответствующее программное обеспечение для анализа данных по массированному секвенированию библиотек Т-клеточных рецепторов и антител, в котором имплементирована возможность учета молекулярных баркодов, маркирующих каждую синтезированную молекулу кДНК, позволяющих нормировать библиотеки для сравнительного анализа.
Ведется работа по доведению программного обеспечения до уровня простоты и надежности, при котором первичный анализ «сырых» данных массированного секвенирования может проводиться силами заинтересованного сотрудника клиники или научной лаборатории — не профессионального биоинформатика (open source, консольный интерфейс).
Мы ожидаем, что применение технологии молекулярного баркодирования позволит радикальным образом повысить качество анализа данных за счет прямой дифференциальной идентификации ошибок ПЦР и реального разнообразия вариабельных участков, более точного количественного анализа, а также за счет нормирования сравниваемых массивов на известное число реальных молекулярных событий.
- Bolotin D.A., Mamedov I.Z., Britanova O.V., Zvyagin I.V., Shagin D., Ustyugova S.V., Turchaninova M.A., Lukyanov S., Lebedev Y.B., Chudakov D.M. (2012). Next generation sequencing for TCR repertoire profiling: platform-specific features and correction algorithms. Eur. J. Immunol. 42,
3073–3083; - Britanova O.V., Bochkova A.G., Staroverov D.B., Fedorenko D.A., Bolotin D.A., Mamedov I.Z., Turchaninova M.A., Putintseva E.V., Kotlobay A.A., Lukyanov S., Novik A.A., Lebedev Y.B., Chudakov D.M. (2012). First autologous hematopoietic SCT for ankylosing spondylitis: a case report and clues to understanding the therapy. Bone Marrow Transplant. 47,
1479–1481.
III. Применение новых технологических подходов в биомедицине
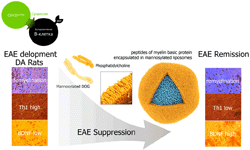
Лаборатория биокатализа — Доклинические испытания инкапсулированных пептидов МВР, подавляющих развитие модели аутоиммунной нейродегенерации
Аутоиммунными заболеваниями в той или иной форме страдает около 5% населения Земли. На настоящий момент клиницисты различают порядка 80 различных видов аутоиммунных нарушений. Среди аутоиммунных заболеваний особое место занимает хроническое нейродегенеративное заболевание аутоиммунной природы — рассеянный склероз (РС). Социально-экономическое и медицинское значение рассеянного склероза (РС) чрезвычайно велико, т.к. из активной жизни исключаются лица наиболее продуктивного и трудоспособного возраста. Проблема лечения рассеянного склероза остается далекой от разрешения, поскольку на сегодняшний день не существует лекарственных препаратов, способных значительно замедлить течение РС. Для разработки лекарств направленного действия необходимо глубокое понимание внутриклеточных процессов, происходящих при возникновении иммунного ответа на собственные антигены. В качестве объекта исследования нами был выбран основной белок миелина, который является одной из основных мишеней иммунной системы при протекании рассеянного склероза. Нами были определены иммунодоминантные фрагменты МВР и эффект их введения в составе липосом на развитие экспериментального аутоиммунного энцефаломиелита (животной модели РС). Иммунодоминантные фрагменты МВР в составе маннозилированных липосом значительно снижали тяжесть заболевания, ингибировали продукцию провоспалительных цитокинов (Th1) в ЦНС и индуцировали ремиелинизацию и синтез нейротропного фактора мозга (BDNF). Пройден полный цикл доклинических испытаний и первая фаза клинических испытаний препарата второго поколения для лечения рассеянного склероза «Миелоксен», созданный на основе полученных данных.
- Belogurov A.A. Jr., Stepanov A.V., Smirnov I.V., Melamed D., Bacon A., Mamedov A.E., Boitsov V.M., Sashchenko L.P., Ponomarenko N.A., Sharanova S.N., Boyko A.N., Dubina M.V., Friboulet A., Genkin D.D., Gabibov A.G. (2012). Liposome-encapsulated peptides protect against experimental allergic encephalitis. FASEB J. Epub ahead of print.
- Защищенное авторское право на изобретение: WO/2011/065867, RU2448685.
Лаборатория протеомики — Поиск пептидных маркеров рака яичника в сыворотке крови человека при помощи протеомных технологий
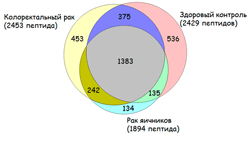
Сформированы каталоги идентифицированных пептидов сыворотки крови практически здоровых доноров и пациентов с колоректальным раком, раком яичников и сифилисом, включающие в себя 3342 структуры. Выявлены пептиды, уникальные для каждой из исследованных патологий.
С целью выявления потенциальных пептидных маркеров ряда социально-значимых заболеваний человека из сыворотки крови практически здоровых доноров и пациентов с различными социально-значимыми заболеваниями проведена работа по выделению и идентификации пептидов тандемной масс-спектрометрией, сопряжённой с ВЭЖХ. В общей сложности было идентифицировано 3342 уникальных (неповторяющихся) пептида, являющихся фрагментами 366 белков. По группам образцов эти цифры распределились следующим образом: здоровые доноры — 2429 пептидов из 230 белков; колоректальный рак — 2453 пептида из 184 белков; рак яичников — 1894 пептида из 159 белков; сифилис — 445 пептидов из 70 белков. Количество уникальных для каждой группы образцов пептидов составило: здоровые доноры — 542 пептида из 105 белков; колоректальный рак — 458 пептидов из 58 белков; рак яичников — 150 пептидов из 35 белков; сифилис — 63 пептида из 19 белков.
Лаборатория нейрорецепторов и нейрорегуляторов — Севанол: новый анальгетик
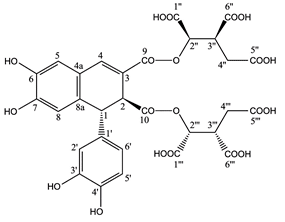
Обнаружен новый анальгетик севанол — низкомолекулярный компонент из экстракта чабреца (Thymus armeniacus), активный по отношению к ASIC3-рецепторам и проявляющий анальгетическую активность в тестах in vivo.
Из уксуснокислого экстракта чабреца (Thymus armeniacus) выделен низкомолекулярный компонент массой 706 Да, получивший название севанол. Севанол — первое природное низкомолекулярное соединение, которое полностью обратимо ингибирует быструю (IC50 353±23 мкM) и частично (~45%) постоянную (IC50 234±53 мкМ) компоненты тока кислото-чувствительного ионного канала 3 типа человека (hASIC3), играющего важную роль в восприятии болевых сигналов периферической нервной системы. Структура севанола установлена методом ЯМР и подтверждена масс-спектрометрией ESI±MS. Севанол представляет собой сложный эфир эпифилловой кислоты и двух остатков изолимонной кислоты и является новым представителем класса полифенольных соединений — лигнанов. Севанол проявляет значительную анальгетическую активность в тестах in vivo. В дозах
- Dubinnyi M.A., Osmakov D.I., Koshelev S.G., Kozlov S.A., Andreev Y.A., Zakaryan N.A., Dyachenko I.A., Bondarenko D.A., Arseniev A.S., Grishin E.V. (2012). Lignan from thyme possessing inhibitory effect on ASIC3 current. J. Biol. Chem. 287,
32993–33000.
Лаборатория клеточных взаимодействий — Миелопептид МП-1 усиливает эффективность цитостатической терапии лимфолейкоза
Миелопептид МП-1 является иммуномодулятором, нормализующим антителообразование в условиях иммунодефицитов различной этиологии. В основе механизма иммунокорригирующего действия МП-1 лежит его способность восстанавливать нарушенный баланс CD4/CD8 клеток. Учитывая способность МП-1 нормализовать баланс основных регуляторных субпопуляций клеток иммунной системы было высказано предположение о возможности применения данного миелопептида для коррекции иммунного статуса, нарушенного процессом опухолеобразования в организме, с целью противодействия развитию опухоли. Проведенные эксперименты с использованием мышиной модели перевиваемого лимфолейкоза Р388 подтвердили указанное предположение. Было продемонстрировано, что миелопептид МП-1 усиливает эффективность цитостатической терапии лимфолейкоза и препятствует росту этой опухоли в условиях иммуносупрессии, вызванной радиационным облучением.
- Фонина Л.А., Белёвская Р.Г., Трещалина Е.М., Беспалова Ж.Д., Ефремов М.А., Седакова Л.А., Кирилина Е.А. (2012). Синтез и противоопухолевые свойства миелопептида МП-1. Биоорганическая химия 38(4),
406–412.
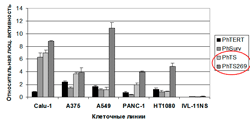
Лаборатория структуры и функций генов человека — Сильные раково-специфичные тандемные промоторы pSurv—pTERT и pTERT—pSurv
Исследованы промоторные свойства тандемных комбинаций двух наиболее широко используемых для целей генной терапии промоторов генов сурвивина pSurv и каталитической единицы теломеразы pTERT. Показано, что в обоих тандемных комбинациях pSurv—pTERT—ген и pTERT—pSurv—ген транскрипционно-активным является промотор, прилегающий к гену. Дистальный промотор утрачивает способность инициировать транскрипцию. Выяснен механизм явления. Показано, что тандемы укороченных промоторов являются наиболее сильными из известных раково-специфичных промоторов и могут служить для создания векторных генно-терапевтических конструкций для использования в онкологии.
- Alekseenko I.V., Pleshkan V.V., Kopantzev E.P., Stukacheva E.A., Chernov I.P., Vinogradova T.V., Sverdlov E.D. (2012). Activity of the Upstream Component of Tandem TERT/Survivin Promoters Depends on Features of the Downstream Component. PLoS One 7, e46474.
Группа кросс-сшивающих ферментов — Структурно-функциональная организация антител G класса в процессе формирования адаптивного иммунитета в норме и при вторичных иммунодефицитах
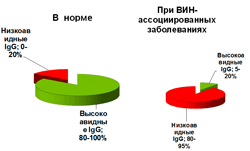
Получена доказательная база существования ранее неизвестной формы вторичной иммунологической недостаточности В-системы иммунитета, обусловленной расстройствами фолдинга антител G класса в плазматических клетках (ПК), ведущих к повышенной секреции (до
На основании статистического и корреляционного анализов созданной базы данных здоровых доноров и пациентов с различными проявлениями ВИН-ассоциированных заболеваний выявлена сильная корреляционная связь авидности антител G класса с клиническими проявления иммунодефицитных синдромов (r=0,83—0,95), а также с показателями Th2 типа иммунного ответа
На основе новых представлений о механизмах формирования адаптивного иммунитета и патогенеза ВИН-ассоциированных заболеваний разработана принципиально новая стратегия диагностики и лечения вторичных иммунодефицитов, не зависящая от природы этиотропных агентов и факторов, влияющих на биообъект.
4 января 2013 года