Пресс-центр / новости / Наука /
Керасомы - стабильные липосомы нового поколения
Проблема доставки противораковых лекарств очень актуальна, потому что практически все применяемые противораковые лекарства плохо растворимы в воде и обладают низкой селективностью по отношению к опухолевым клеткам, что приводит к появлению побочных эффектов. Наиболее известными наноносителями для доставки лекарств, которые позволяют частично решить эти проблемы, и которые уже нашли свое место на фармацевтическом рынке, являются липосомы. Однако при всех своих достоинствах липосомы не обладают достаточной стабильностью для длительного циркулирования в кровотоке. В Лаборатории биомедицинских материалов ИБХ РАН (под руководством д.х.н. Марквичевой Е.А.) совместно с коллегами из Московского технологического университета (кампус МИТХТ) создали 4 типа липосом нового типа - керасом, которые отличаются повышенной стабильностью и способны обеспечить пролонгированное высвобождение различных лекарств, в частности доксорубицина. Результаты исследования опубликованы в журнале Materials Science & Engineering C.
Поскольку практически все применяемые сегодня противораковые лекарства плохо растворимы в воде, обладают низкой селективностью по отношению к опухолевым клеткам, и, как следствие, дают побочные эффекты, существует необходимость создания новых наноразмерных систем их доставки. Наноносители, загруженные лекарством, попадают в опухолевые клетки путем пассивной доставки благодаря так называемому Enhanced Permeability and Retention (EPR) эффекту. При этом они должны циркулировать в кровотоке в течение достаточно продолжительного времени. Наиболее известными наноносителями, которые уже нашли свое место на фармацевтическом рынке, являются липосомы, которые при всех их достоинствах не обладают достаточной стабильностью для решения этой задачи.
В Лаборатории биомедицинских материалов ИБХ РАН (под рук. Е.А. Марквичевой) совместно с коллегами из Московского технологического университета (кампус МИТХТ) ведутся исследования по созданию нового типа стабильных липосом – керасом (рис. 1). Про керасомы рассказывает один из авторов статьи Анастасия Гилева : ”Керасомы представляют собой катионные липосомы, покрытые кремний-органической оболочкой. Остеклованная поверхность керасом позволяет существенно увеличить их стабильность по сравнению с обычными липосомами и, как следствие, время циркуляции в кровотоке. Стабильность керасом можно регулировать путем варьирования липидного состава. В керасомы можно инкапсулировать лекарство или генетический материал, а положительный заряд на их поверхности обеспечивает взаимодействие с отрицательно заряженной поверхностью клетки”.
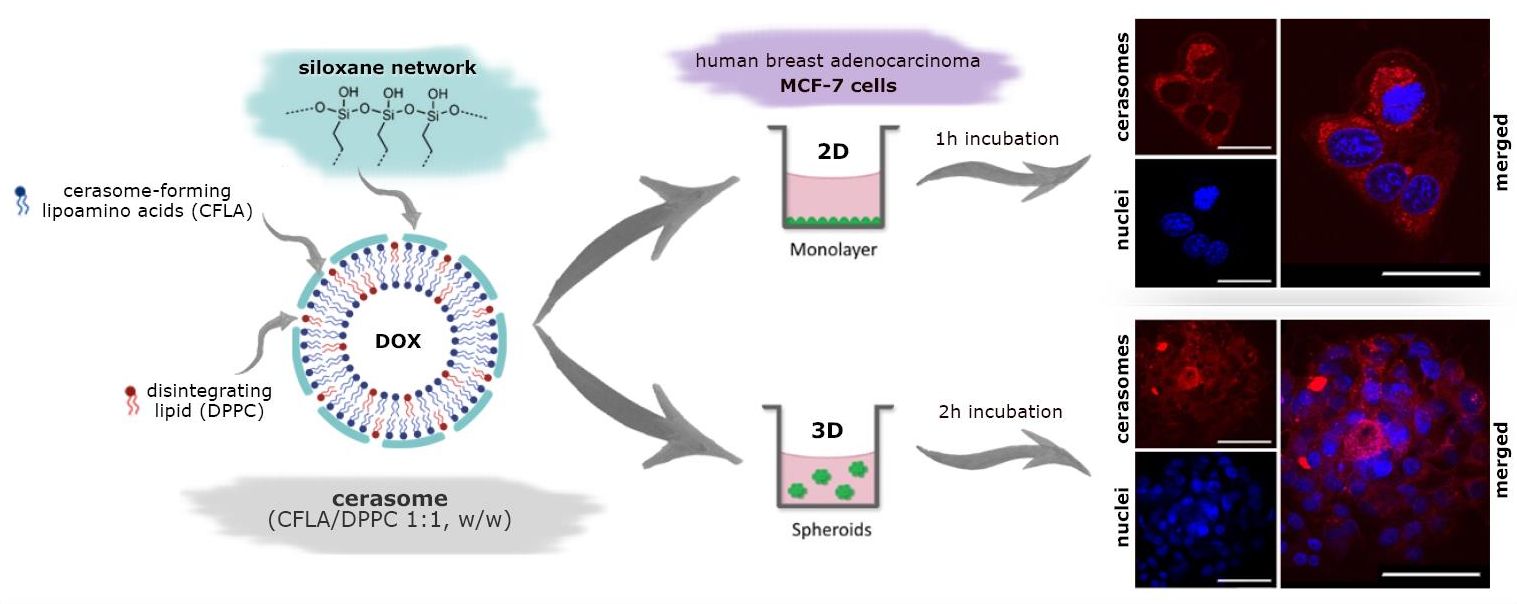
Рис. 1. Керасомы как система EPR-опосредованной доставки противоопухолевого препарата доксорубицина (DOX).
Для формирования керасом используют молекулы липидной природы, к полярной группе которых ковалентно пришиты различные силоксановые производные. Мы разработали схему синтеза катионных и нейтральных керасом-образующих липоаминокислот (cerasome-forming lipoamino acids, CFLA) на основе природных аминокислот и высших жирных спиртов. Были синтезированы нейтральные (незаряженные) и катионное CFLA и на их основе сформированы «чистые» керасомы (только из CFLA) и «смешанные» керасомы из смеси CFLA с разрыхляющим липидом дипальмитоилфосфатидилхолином (DPPC) (1:1, % масс). Таким образом, получили четыре типа керасом, загруженных модельным противоопухолевым препаратом доксорубицином (DOX): нейтральные «чистые», катионные «чистые», нейтральные «смешанные» и катионные «смешанные» керасомы.
Использование катионных CFLA позволило увеличить заряд формируемых частиц в 4 и 6 раз в случае «чистых» и «смешанных» керасом, соответственно. Введение разрыхляющих липидов DPPC привело к увеличению в 1,5 раза диаметра формируемых керасом и снижению больше чем в 2 раза их ζ-потенциала. «Чистые» керасомы были стабильны более 120 дней, тогда как «смешанные» - в течение 30 дней, что, тем не менее, минимум в два раза превышает стабильность обычных липосом.
Для изучения влияния липидного состава керасом на эффективность высвобождения DOX был исследован набор нейтральных керасом, различающихся по липидному составу и содержанию (или отсутствию) в них DPPC. Обнаружили, что лекарство быстрее всего высвобождалось из обычных липосом и «смешанных» CFLA/DPPC керасом. При этом уменьшение содержания DPPC в керасомах приводило к снижению количества вышедшего лекарства. Существенную разницу между профилями высвобождения DOX из «чистых» и «смешанных» керасом можно объяснить достаточно быстрой деградацией DPPC в «смешанных» керасомах, которая приводила к образованию пор в силоксановой сети. Отсутствие же DPPC в «чистых» керасомах, наоборот, способствовало медленному разрушению остеклованной поверхности наночастиц и, тем самым, пролонгированному высвобождению лекарства.
Для исследования эффективности накопления керасом в клетках и их цитотоксичности использовали линию клеткок аденокарциномы молочной железы человека MCF-7. Известно, что в большинстве лабораторий для оценки эффективности противоопухолевых препаратов in vitro используется монослойная культура клеток (2D модель). Однако эта модель не отражает сложных взаимодействий «клетка-клетка» и «клетка-внеклеточный матрикс» и, следовательно, не способна имитировать солидную опухоль (от англ solid) in vivo. В настоящее время существует несколько коммерчески доступных методов получения опухолевых сфероидов (3D модель), которые являются более адекватными in vitro моделями для тестирования наноносителей. В нашей работе для формирования 3D сфероидов использовался простой и универсальный подход, недавно разработанный нами вместе с Лабораторией новых методов синтеза пептидных лекарственных препаратов (МБНПК Цитомед, Санкт-Петербург, Россия). Он основан на эффекте самосборки раковых клеток в сфероиды под действием пептида, содержащего RGD-последовательность аминокислот, при его добавлении непосредственно к монослойной культуре клеток.
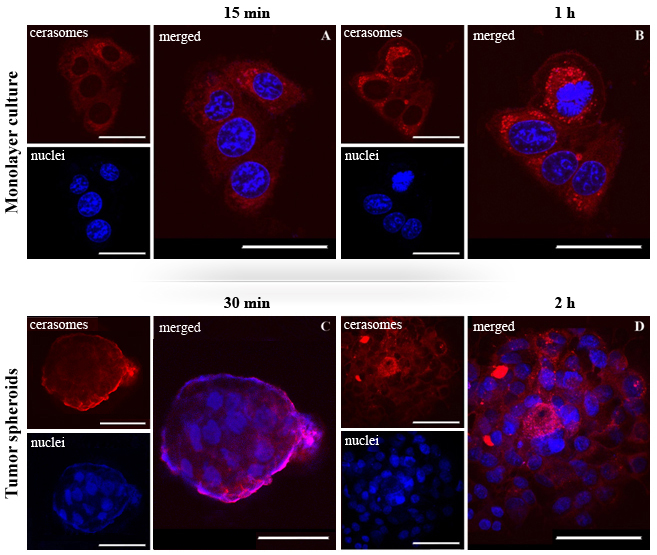
Рис. 2. Клетки MCF-7 после инкубации со «смешанными» катионными керасомами: монослойная культура через 15 мин (A) и 1 ч (B); опухолевые сфероиды через 30 мин (C) и 2 ч (D). Красный – керасомы (DOX), синий – ядра клеток (Hoecsht 33258). Размерная шкала - 50 мкм.
Эффективность накопления керасом в клетках изучали с помощью конфокальной микроскопии (рис 2.). Показано, что катионные керасомы («смешанные» и «чистые») накапливались в клетках значительно эффективнее, чем нейтральные керасомы. Введение DPCC в состав «смешанных» керасом не влияло на эффективность их накопления в клетках. В случае 2D модели катионные керасомы проникали в клетки уже через 15 мин, тогда как нейтральные - после 1 ч инкубации. В случае 3D модели проникновение керасом во все клетки, в том числе и клетки, локализованные в центре сфероида, происходило медленнее. Так, катионные керасомы достигали центра сфероида через 1,5-2 ч инкубации со сфероидами, в то время локализацию там нейтральных керасом наблюдали только через 3,5-4 ч.
Исследование цитотоксичности керасом показало, что максимальную цитотоксичность имели «смешанные» катионные керасомы, что, вероятно, связано с накоплением их в клетках в больших количествах, чем других образцов керасом. «Чистые» керасомы не проявляли токсичности даже после 48 ч при любых исследованных концентрациях DOX, а вызывали гибель клеток при достаточно высоких концентрациях лекарства только через 72 ч. Это можно объяснить их высокой стабильностью и медленным высвобождением инкапсулированного препарата.
Таким образом, разработанные нами керасомы представляют собой перспективную стабильную систему EPR-опосредованной доставки противоопухолевых препаратов. Такая система может быть легко адаптирована и способна обеспечить пролонгированное высвобождение различных лекарств. Результаты исследования опубликованы в журнале Materials Science & Engineering C.
12 апреля 2019 года

