Пресс-центр / новости / Наука /
Выявлена важная роль цинка в работе рецептора TLR1 системы врожденного иммунитета
Толл-подобные рецепторы являются ключевыми участниками врожденного иммунитета. Несмотря на большое количество исследований и данных об этих белках, структурно-функциональные основы их работы до сих пор не до конца ясны. Сотрудники лаборатории биомолекулярной ЯМР-спектроскопии, лаборатории биоинформационных методов комбинаторной химии и биологии ИБХ РАН совместно с коллегами из МФТИ и Чанчуньского института прикладной химии (КНР) выявили важную роль цинка в работе толл-подобного рецептора 1 и предложили возможные механизмы цинк-опосредованной активации рецептора. Работа выполнена при поддержке гранта РФФИ 20-34-70024 и опубликована в журнале Communications Biology.

Lushpa VA, Goncharuk MV, Lin C, Zalevsky AO, Talyzina IA, Luginina AP, Vakhrameev DD, Shevtsov MB, Goncharuk SA, Arseniev AS, Borshchevskiy VI, Wang X, Mineev KS
Толл-подобные рецепторы (TLR) принимают участие во врожденном иммунном ответе и служат мишенями при разработке лекарств против воспалительных, нейродегенеративных и аутоиммунных заболеваний. Общая картина развития иммунного ответа через TLR известна: после распознавания молекулы, характерной для патогена, рецепторы TLR начинают образовывать димеры и активировать специализированные внутриклеточные белки (адаптеры). Например, попадание патогенной бактерии в организм приводит к появлению в межклеточной среде компонентов их клеточной стенки, которые связываются с TLR1 и TLR2 и запускают образование комплекса TLR1/TLR2. Последний, в свою очередь, передает сигнал внутрь клетки и в результате происходит выброс цитокинов (белков-регуляторов иммунного ответа). Несмотря на общее понимание процесса, многие его детали остаются неизученными, в частности, до сих пор не ясно как же сигнал передается внутрь клетки, почему именно димер цитоплазматического домена (TIR) TLR способен активировать внутриклеточные каскады реакций, каковы структурные основы взаимодействия TIR доменов.
Чтобы приблизиться к ответам на данные вопросы было проведено комплексное исследование структуры TIR домена TLR1. Для этого пространственная структура домена была определена двумя методами - ЯМР-спектроскопии в растворе и рентгеноструктурного анализа в кристаллах (Рисунок 1). Сравнение структур выявило отличие в области, содержащей два остатка цистеина, что навело ученых на мысль о существовании возможного взаимодействия домена рецептора с ионами цинка (SH-группы цистеинов чаще всего формируют сайт связывания для этого металла во внутриклеточных белках) .
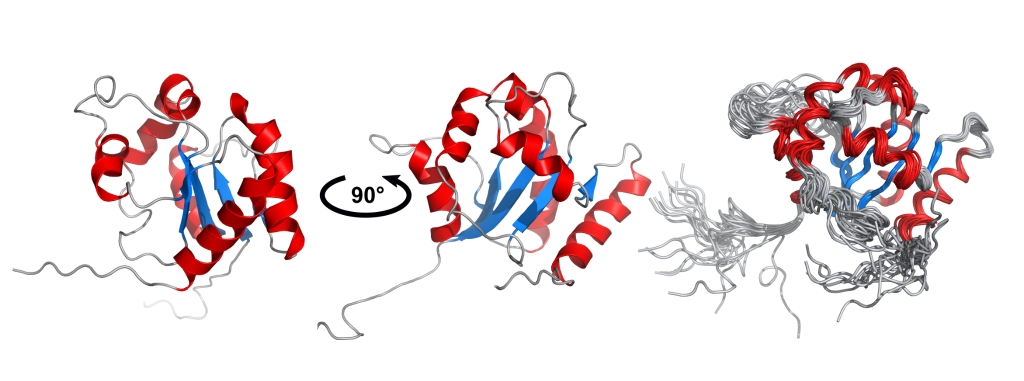
Рисунок 1. Пространственная структура TIR домена TLR1 по данным ЯМР спектроскопии.
Для проверки этой гипотезы была проведена серия экспериментов по изучению связывания TIR домена с ионами различных металлов, содержащихся в цитоплазме клетки. Выяснилось, что в то время как остальные металлы не взаимодействовали с доменом, цинк связывается с TIR доменом специфически в наномолярных концентрациях. Кроме того, оказалось, что происходит образование двух конкурирующих комплексов TLR1/Zn.
Так как напрямую получить структуры комплексов TLR1/Zn не удалось, были использованы подходы на основе точечного мутагенеза белка и компьютерного моделирования. Удалось показать, что один из комплексов образуется за счет цистеинов C667 и C686, в то время как второй комплекс зависит только от наличия С667. Для двух вариантов взаимодействия были получены модели с использованием молекулярной динамики (Рисунок 2). Компьютерный эксперимент показывает, что цинк может стабилизировать важный участок TIR домена в двух различных состояниях.
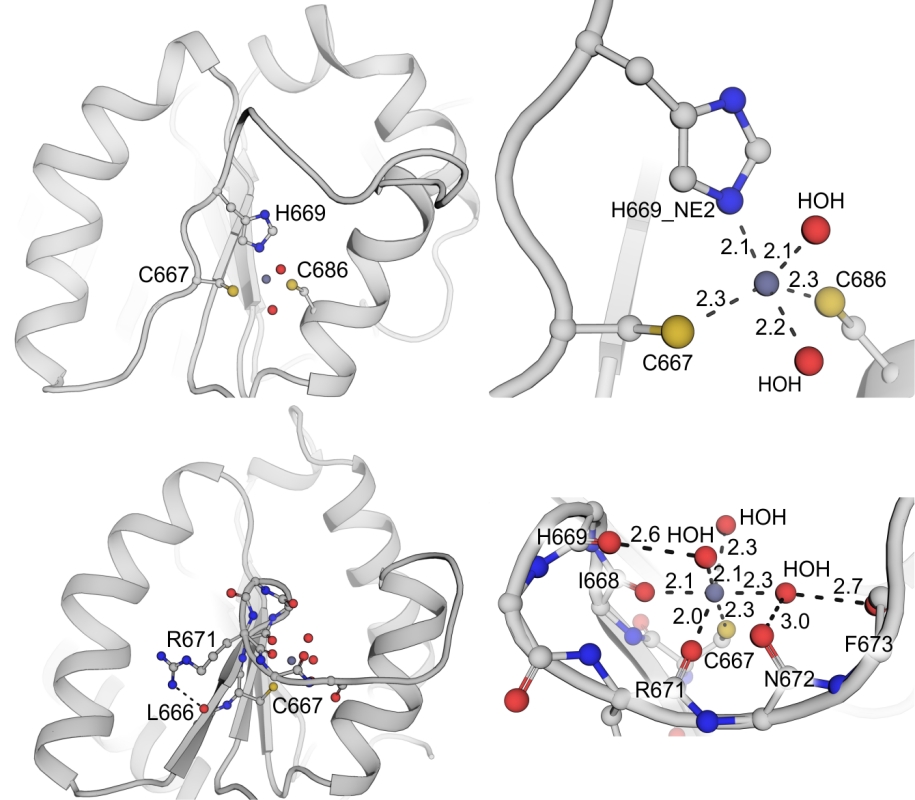
Рисунок 2. Модели двух различных цинк-связанных форм TIR домена рецептора TLR1.
Чтобы понять, насколько обнаруженное взаимодействие белка с цинком важно для работы рецептора, была изучена активность TLR1 в живых клетках. Ученые показали, что изменение концентрации цинка влияет на активность TLR1, а мутация остатка цистеина 667 приводит к полной потере активности рецептора. Обобщая полученные результаты авторы предполагают, что цинк-связывающая способность TIR домена TLR1 является критически важной для функционирования белка.
24 августа 2021 года

