Группа анализа и коррекции генома
|
Руководитель: Патрушев Л.И. |
Лаборатория изучает роли некодирующих последовательностей генома человека в связи с распространенными многофакторными заболеваниями.
Основные объекты исследования:
- Размер генома эукариот («Парадокс С», «Загадка С»).
- Интронные микроРНК генов протромбина, а также природных антикоагулянтов – протеина C и протеина S в связи с их возможным участием в регуляции экспрессии генов системы свертывания крови и развитии тромбофилий.
- Ген опухолевого супрессора PTEN и его псевдоген PTENP1. Их экспрессия в норме, при раке и гиперплазиях эндометрия как потенциальный биомаркер этого заболевания.
- Клинический материал больных тромбозами и раком эндометрия в рамках помощи практикующим врачам лечебных учреждений г. Москвы.
Прикладные исследования: Системы ДНК-диагностики тромбофилий, высокоочищенная Taq-ДНК-полимераза, бактериальные продуценты аналогов инсулина.
Лаборатория ведет постоянное научное сотрудничество с ведущими клиниками и медицинскими исследовательскими центрами г. Москвы.
Группа осуществляет постоянное сотрудничество с ведущими клиниками и медицинскими исследовательскими центрами г. Москвы, а также сотрудничает с рядом НИИ: Научно-исследовательский институт ревматологии им. В.А. Насоновой, Научный центр неврологии Первый Московский государственный медицинский университет им. И.М. Сеченова, Российский национальный исследовательский медицинский университет им. Н.И. Пирогова и Российская медицинская академия последипломного образования.
Педагогическая работа:
- 30-часовой курс лекций по современным методам генной инженерии, который регулярно читается студентам, магистрантам и аспирантам МГУ, МФТИ и других учебных заведений г. Москвы и г. Пущино Московской области. Написаны две монографии, включающие главы учебного характера.
- Две монографии, включающие главы образовательного характера.
- Научное руководство (консультирование) кандидатскими и докторскими диссертациями, а также курсовыми и дипломными работами студентов.

Студенты четвертого курса кафедры биоорганической химии МГУ, кафедры физико-химической биологии и биотехнологии Московского физико-технического института, а также аспиранты второго года обучения Учебно-научного центра ИБХ РАН после окончания курса лекций по генной инженерии. Москва, ИБХ РАН, декабрь 2015 г.

Магистранты 2-го года обучения после окончания курса лекций по генной инженерии. Институт белка РАН, г.Пущино Московской области, декабрь 2016 г.
Под научным руководством или при научном консультировании Л.И. Патрушева защищено 7 диссертаций.
Участие в общественных мероприятиях:
- Постоянное участие в Российских и международных конференциях, а также в Российском антитромботическом форуме.

II Международная научная конференция «Генетика и биотехнология XXI века: проблемы, достижения, перспективы», посвящённая 50-летию основания Института генетики и цитологии НАН Беларуси. 13-16 октября 2015 года, Минск, Республика Беларусь.

II Международная научная конференция «Генетика и биотехнология XXI века: проблемы, достижения, перспективы», посвящённая 50-летию основания Института генетики и цитологии НАН Беларуси. 13-16 октября 2015 года, Минск, Республика Беларусь.

V Съезд биохимиков России. Сочи-Дагомыс, Россия 4-8 октября 2016. Стендовый доклад: «Исследование метилирования 5’-концевой области псевдогена PTENP1 у пациенток с гиперплазией и раком эндометрия» (Т.Ф. Коваленко, И.А. Лапина, К.В. Морозова, Л.А. Озолиня, Л.И. Патрушев) отмечен, на Съезде биохимиков как один из лучших.
- Чтение просветительских лекций.

Руководитель Группы Л.И. Патрушев – член Ученого и Диссертационного Советов ИБХ РАН, рецензент Российского научного фонда (РНФ) и Российского фонда фундаментальных исследований (РФФИ).
Попробуем на пальцах! «Геном и жизнь: почему мы такие разные?» https://vimeo.com/52368241, https://public.wikireading.ru/42507
Финансирование:
- Гранты РФФИ: 11-08-00550, 14-08-00801.
- Договоры подряда на производство наукоемкой продукции.
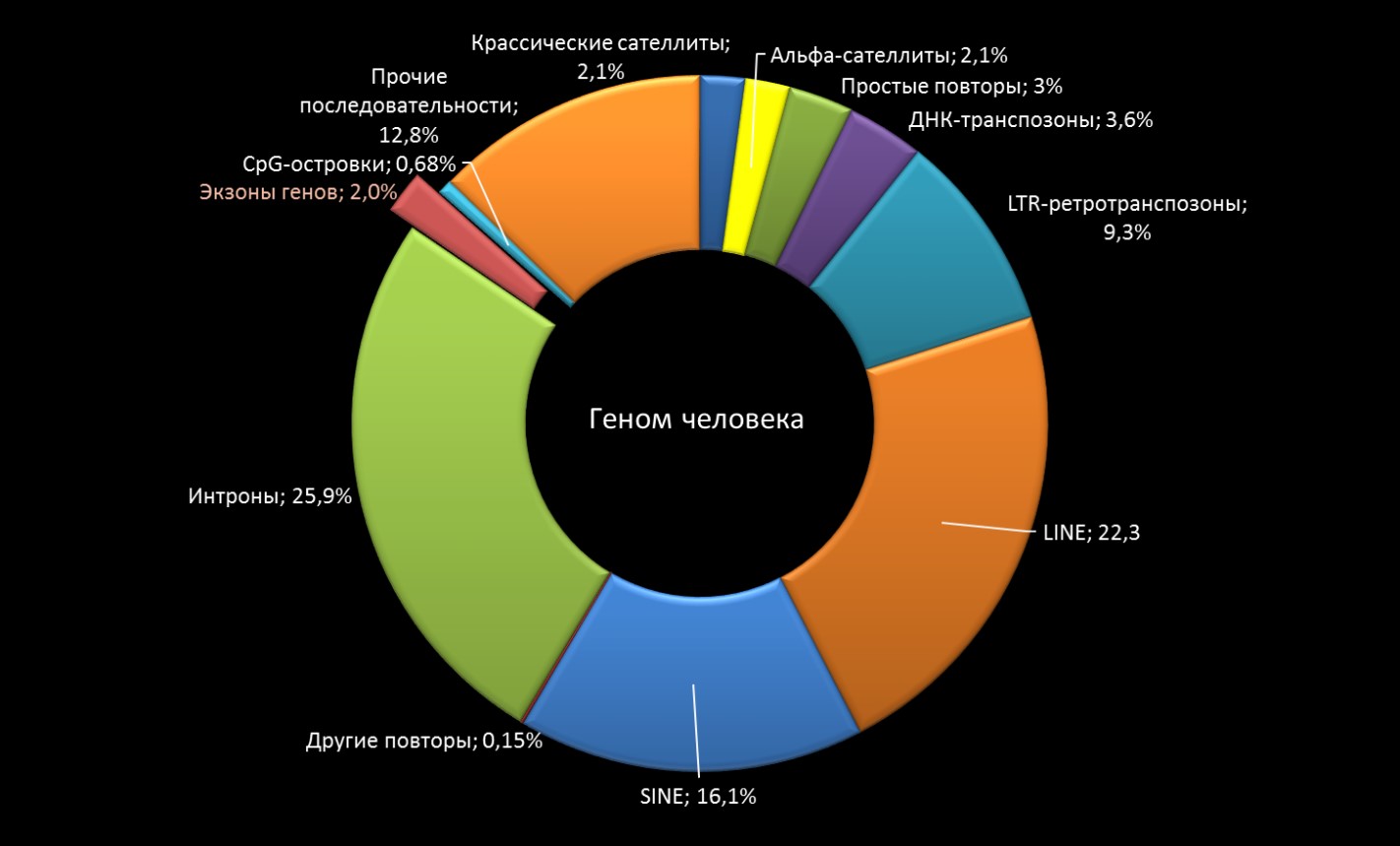
Суммарное содержание ДНК в гаплоидном наборе хромосом (в ядре гаметы) разных эукариотических видов, обозначаемое латинским символом «C» (размер их генома), различается более, чем в 200 000 раз. У позвоночных одними из самых больших геномов обладают хвостатые амфибии и двоякодышащие рыбы – по ~120 пг ДНК. (Для сравнения – размер генома человека составляет 3,5 пг.) У наземных растений гигантские геномы обнаруживают представители лилейных (Fritillaria assyriaca – ~127 пг). 1 Пг ДНК соответствует ~1000 м.п.н. Несоответствие между размером генома и фенотипической сложностью организма, который им обладает, получило название «парадокса C» (C-value paradox). При этом основная масса ДНК больших геномов эукариот представлена нуклеотидными последовательностями, не кодирующими белки и РНК. В частности, доля кодирующих частей генов в геноме человека составляют лишь ~3%.

Парадокс C. C.A. Thomas, 1971 г. Размер генома не коррелирует с биологической сложностью видов (их положением в эволюционной иерархии биологических видов). Размеры генома: Кузнечик – 17 pg, Лошадь – 3,2 pg, Человек – 3,5 pg, Южноамериканская двоякодышащая рыба Lepidosiren paradoxa – 120 pg. 1 pg ДНК = 1000 млн.п.н.
Проведенный нами теоретический анализ проблемы вариабельности размеров генома эукариот выявил у некодирующих последовательностей наличие дополнительной функции в составе новой (выделяемой нами третьей) системы защиты кодирующих последовательностей от мутаций, вызываемых химическими мутагенами. При этом, в соответствии с нашей концепцией, именно эндогенные мутагены создают постоянные условия, в которых эволюционирует эукариотический геном. Действительно, по имеющимся данным, одни только активные формы кислорода вызывают 50-200 тыс. повреждений ДНК ежедневно в каждой клетке организма человека. Избыточные некодирующие последовательности в этой системе выполняют роль ловушек химических мутагенов. Данная высокодинамичная система, функционирующая в тесном взаимодействии с двумя другими системами (антимутагенеза и репарации повреждений ДНК), вносит весьма существенный вклад в общую защиту генома (см. рисунок 1).
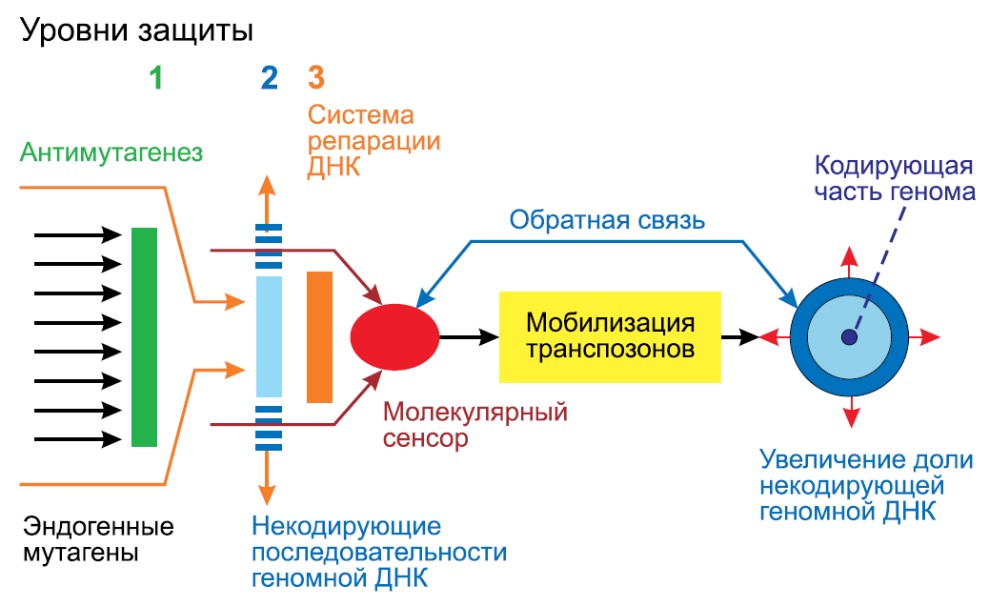
Рис. 1. Предполагаемый механизм контроля содержания некодирующей ДНК в эукариотическом геноме. Изображены три уровня защиты эукариотического генома от эндогенных химических мутагенов (горизонтальные черные стрелки слева), которые сформированы 1) системой антимутагенеза (зеленый прямоугольник), 2) некодирующие последовательности геномной ДНК (синий прямоугольник) и 3) системой репарации ДНК (оранжевый прямоугольник). В том случае, если все три системы не обеспечивают необходимой защиты генов, происходит мутационное изменение гипотетического молекулярного сенсора(ов) (красный овал), что сопровождается мобилизацией транспозонов, увеличением некодирующей части генома и снижением частоты возникновения спонтанных мутаций до исходного оптимального уровня. Кодирующая часть генома изображена темно-синей точкой в центре голубого круга, а тонкие красные стрелки указывают на увеличение размера генома.
В соответствии с нашими расcчетами, одно только наличие некодирующей части в геноме человека обеспечивает ему ~100-кратную защиту кодирующих последовательностей от химических мутагенов разной природы. У организмов с большими геномами некодирующие последовательности могут обеспечивать основную защиту от эндогенных химических мутагенов, а системы антимутагенеза и репарации работать хуже, что в целом обеспечивает у них приемлемый уровень частот спонтанных мутаций в кодирующих частях генов.
Концепция ксенобиоза и эндогенных ксенобиотиков
В рамках разработанной концепции предполагается, что соматические мутации могут изменять первичную структуру полипептидных цепей ферментов таким образом, что они начинают распознавать эндогенные метаболиты в качестве новых субстратов и метаболизировать их с образованием новых химических соединений, не свойственных данному организму – эндогенных ксенобиотиков. Гипотетический глобальный процесс образования эндогенных ксенобиотиков по этому механизму мы называем ксенобиозом. Концепция развивается на примере системы цитохрома P-450 и абзимов. Так, система цитохрома P-450, обладающая широкой субстратной специфичностью, распознает и метаболизирует миллионы экзогенных химических соединений, но, в то же время, толерантна к эндогенным метаболитам, многие из которых структурно напоминают экзогенные ксенобиотики. Измененный соматическими мутациями цитохром P-450 мог бы метаболизировать, в частности, ароматические аминокислоты по эпоксид-диольному пути с образованием эндогенных мутагенов и появлением у соматических клеток мутаторного фенотипа. Постепенное накопление мутаций должно сопровождаться старением клеток, возрастанием риска их малигнизации и развитием системных многофакторных заболеваний.
Интронные микроРНК
С помощью близнецового метода и семейного анализа установлено, что генетические факторы составляют ~60% всех факторов риска венозных и артериальных тромбозов. Несмотря на интенсивные поиски генетических маркеров этих заболеваний, они остаются недостаточно изученными. В этой связи целью наших исследований является поиск новых регуляторов и генетических маркеров системы свертывания крови среди интронных миРНК генов протромбина, а также природных антикоагулянтов протеина C и протеина S.
МикроРНК (миРНК) представляют собой короткие рибонуклеотидные последовательности длиной 19-22 нт, участвующие в регуляции экспрессии эукариотических генов, в основном, на посттранскрипционном уровне. Более 40% из нескольких тысяч известных миРНК локализовано в интронах генов. Нарушения биосинтеза и функциональной активности многих миРНК часто ассоциированы с многофакторными заболеваниями человека, включая рак, аутоиммунные и нейродегенеративные патологии, а также тромбозы. В рамках исследования, направленного на поиск новых генетических маркеров, ассоциированных с тромбофилиями, нами биоинформатическими методами в интронах генов протромбина, а также природных антикоагулянтов – протеина C и протеина S было обнаружено 29 предполагаемых предшественников миРНК, высокогомологичных известным природным предшественникам. Для подтверждения функциональной значимости выявленных последовательностей сконструирован миниген зеленого флуоресцирующего белка TurboGFP, содержащий искусственный интрон длиной в 61 п.н., введенный в ген gfp, находящийся под контролем цитомегаловирусного промотора в составе экспрессирующей плазмиды pTurboGFP-N (Евроген, Россия) (рис. 2). Такой компактный интрон содержал канонические последовательности 5’- и 3’-концевых сайтов сплайсинга, точки ветвления и полипиримидинового тракта. В центральную часть искусственного интрона были введены два уникальных сайта рестрикции для последующего клонирования анализируемых последовательностей ДНК. Введение по этим сайтам фрагмента ДНК, содержащего предшественник миРНК, сопровождалось вырезанием соответствующей последовательности из образующейся химерной РНК в результате нормального сплайсинга в трансфицированных клетках человека, восстановлением нативной мРНК TurboGFP и свечением клеток в зеленой области спектра. Прохождение адекватного процессинга известного предшественника миРНК hsa-mir5096 с образованием зрелой миРНК было подтверждено разными методами. В настоящее время проводится систематическое исследование обнаруженных последовательной на функциональность.
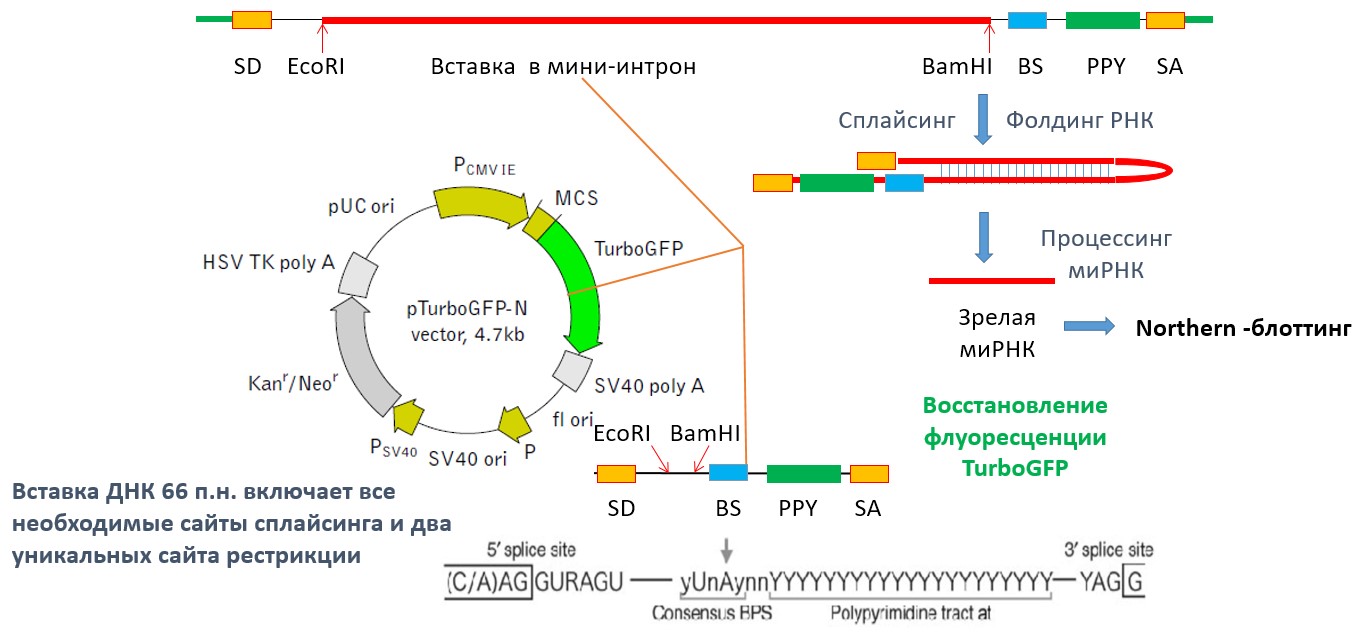
Рис. 2. Миниген turboGFP с искусственным мини-интроном как основа системы для исследования функциональности последовательностей предполагаемых предшественников микроРНК. В структурную часть гена TurboGFP, транскрибируемого с промотора цитомегаловируса в составе плазмиды, встроена короткая последовательность (66 п.н.) содержащая все необходимые сайты сплайсинга, а также три уникальных сайта рестрикции для клонирования исследуемых фрагментов ДНК. При наличии в них гена функционального предшественника миРНК в результате его транскрипции в трансфицированных клетках человека синтезируется сам предшественник, который претерпевает процессинг с образованием зрелой миРНК, активность которой может быть определена в стандартных тестах. SD и SA – донорный и акцепторный сайты сплайсинга, BS – точка ветвления, PPY – полипиримидиновый тракт.
Экспрессия гена опухолевого супрессора PTEN и его псевдогена PTENP1 в норме, а также при раке и гиперплазиях эндометрия
Опухолевый супрессор PTEN контролирует многие клеточные функции, включая клеточный цикл, апоптоз, старение, транскрипцию и трансляцию мРНК многих генов, и он часто инактивируется генетическими мутациями и эпимутациями в клетках различных опухолей. Целью данного направления исследований является изучение влияния метилирования гена PTEN и его псевдогена PTENP1 на их экспрессию в нормальных и опухолевых тканях человека, а также возможности использования этого параметра в качестве генетического маркера гиперплазий (ГЭ) и рака (РЭ) эндометрия. На первом этапе метилирование 5’-концевых участков вышеупомянутых последовательностей исследовали с помощью метилчувствительной ПЦР в геномной ДНК, выделенной из тканей 57 злокачественных опухолей и 43 гиперплазий эндометрия, нормальных тканей 24 женщин в возрасте 17-34 лет и 19 женщин в возрасте 45-65 лет, а также из 20 образцов периферической венозной крови больных РЭ. Установлено, что ни в одном из исследованных образцов ДНК ген PTEN не был метилирован. В отличие от этого, метилирование псевдогена PTENP1 было обнаружено во всех исследованных тканях, кроме периферической крови. Сравнение частот метилирования PTENP1 в группах РЭ и ГЭ с таковыми контрольной группы женщин пожилого и среднего возраста не выявило достоверных различий между ними. Во всех группах уровень метилирования был высоким (68-77% у пациенток против 58% в контрольной группе). При этом были обнаружены достоверные различия в частотах метилирования PTENP1 в нормальном эндометрии молодых (4%) и пожилых (58%) женщин. Таким образом установлено, что метилирование псевдогена PTENP1 отражает возрастные изменения в организме человека и может быть не связанным прямо с исследуемой патологией эндометрия. Предполагается, что в зависимости от влияния метилированного PTENP1 на экспрессию гена PTEN метилирование псевдогена может защищать организм от развития РЭ и/или служить маркером предракового состояния клеток эндометрия. Проводится исследование влияния метилирования PTENP1 на экспрессию данного псевдогена, а также гена PTEN в различных клеточных линиях человека.
Прикладные исследования
Системы ДНК-диагностики тромбофилических состояний организма человека
С целью оказания помощи практикующим врачам ведущих Московских клиник в оценке тромбофилических состояний организма пациентов нами разработаны 13 оригинальных тест-систем на основе полимеразной цепной реакции (ПЦР) в режиме реального времени и соответствующих наборов химических реагентов, которые позволяют обнаруживать в геноме человека следующие мутации (SNP), ассоциированные с тромбофилиями или влияющие на метаболизм антикоагулянта варфарина: FV Leiden (ген фактора V), 20210G>A (ген протромбина), 10034 С>Т (ген фибриногена γ), 677C>T (ген 5,10-метилентетрагидрофолатредуктазы), 4G/5G в гене PAI-1 (ген ингибитора активатора плазминогена-1), 10976G>A (ген фактора VII), 807С>Т в гене GpIa (ген гликопротеина I), 1565Т>С в гене GpIIIa (ген гликопротеина III), аллели CYP2C9*2 и *3 (ген цитохрома Р450 CYP2C9), 1639G>A в гене VKORC1 (ген субъединицы эпоксидредуктазы витамина К), I/D-полиморфизм в гене ACE (ген ангиотензинконвертирующего фермента). Группа оказывает постоянную поддержку клиницистам в генотипировании пациентов по вышеупомянутым мутациям.
Высокоочищенная рекомбинантная Taq-ДНК-полимераза
Получен штамм E.coli, продуцирующий рекомбинантную Taq-ДНК-полимеразу. Препараты чистого или модифицированного для горячего старта ПЦР рекомбинантного фермента используются во всех фундаментальных и прикладных исследованиях, проводимых в группе, а также востребованы сторонними организациями.
Бактериальные штаммы-продуценты аналогов проинсулина
Получены бактериальные штаммы-продуценты аналогов проинсулина Lyspro, Aspart и GLARGIN, используемые в биотехнологическом производстве инсулина.
| ФИО | Должность | Контакты |
|---|---|---|
Ранее здесь работали | ||
| Патрушева Н.Л. | ||
 Загрузка...
Загрузка...Научные проекты
 Загрузка...
Загрузка...Патрушев Л.И.
Москва, ул. Миклухо-Маклая, 16/10 — На карте
 Загрузка...
Загрузка...
