Пресс-центр / новости / СМУ /
Видеозапись 19-го семинара СМУ «Фотоиндуцированные процессы во флуоресцентных белках. От сверхбыстрого к сверхмедленному»
Способность биологических молекул воспринимать свет — одна из замечательных их особенностей. Кирилл Солнцев — заведующий лабораторией в технологическом институте Джорджии (Атланта, США) — 19 июня 2014 года рассказал о своих последних исследованиях в области фотоиндуцированных процессов во флуоресцентных белках.
В докладе были рассмотрены фотоиндуцированные процессы переноса протона и электрона, а также изомеризации хромофора в различных классах флуоресцентных белков. Полный фотоцикл флуоресцентных белков простирается на огромный временной диапазон, от фемтосекунд до секунд. Особое внимание лектор уделил исследованию динамики этих фотоциклов и их использованию на практике. В качестве примеров были рассмотрены оптическая модуляция, образование токсичных радикалов и влияние ионов кальция на фотоперенос протона внутри белка. Визит К.М. Солнцева в Россию с серией докладов поддержан фондом «Династия».
Аннотация от автора — Кирилла Солнцева, старшего научного сотрудника химического факультета технологического института Джорджии:
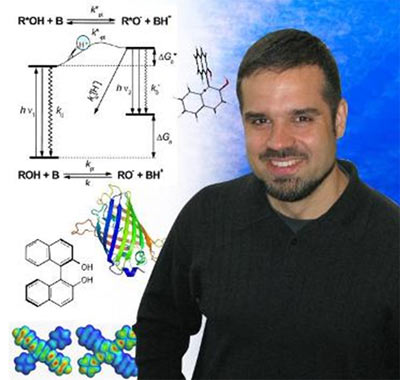
This talk covers the new results from the Solntsev lab for the period of last two years. For the last decade, our research in excited-state processes has concentrated predominantly on excited-state proton transfer (ESPT). While this area continues to provide a rich vein of new reactivity, most recently our methods have been extended to photoacids in biology, taking advantage of the unique mechanism of the green fluorescent protein (GFP). This protein is one of the few recognized examples of the ESPT in nature. The unique rigid β-barrel structure of the protein makes it an ideal system to study proton transfer in a geometrically rigorously well-defined environment.
The first part of the talk deals with the ESPT studies in the GFP and its mutants in the wide range of temperatures and pressures. A unique diffusion-influenced reversible ESPT is observed inside the β-barrel. By point mutations we have modulated the ESPT efficiency along the proton wire. The ESPT in fluorescent proteins (FPs) can be utilized for calcium ion sensing. Addition of Ca2+ inhibited the proton transfer both in ground and in the excited-state. Also, Ca2+ exhibits a strong inhibition on the ESPT non-adiabatic geminate recombination in protic (vs. deuteric) medium.
In the second part of the talk I enter the Terra Incognita of microseconds-to-seconds dynamics in the FPs. The time-resolved-measurements of FPs in this time domain are relatively rare, and mostly involve the Fluorescence Correlation Spectroscopy (FCS), single-wavelength phosphorescence, and single-wavelength transient absorption (TA) measurements. Therefore, no full spectral information about the transients appearing at these times is available, and the mechanistic details of photoinduced processes in FPs at ms—s time scale are unknown. We for the first time have performed broadband transient absorption measurements in the µs—s time scale, to identify the dark states in the series of blue, green and red fluorescent proteins. The complete photocycles of these proteins spanning for fifteen orders of time magnitude were established. The mechanism underlying the absorption relaxation kinetics, including the intraprotein proton transfer, the chromophore isomerization and photoionization is discussed. While most of the fluorescent proteins are used as non-invasive inert fluorescent markers, a mutant of the red fluorescent protein named KillerRed has been found to be strongly phototoxic. A mechanism of its radical-based ROS formation and phototoxicity will be discussed.
References
- Zhou, Y. et al. J. Phys. Chem. B 2014, 118, DOI : 10.1021/jp501707n
- Vegh, R. B. et al. J. Phys. Chem. B 2014, 118, 4527
- Makarov, N. S. et al. J. Photochem. Photobiol. A 2014, 280, 5
- Jablonski, A. E. et al. J. Am. Chem. Soc. 2013, 135, 16410
- Sarkisyan, K. S. et al. Nat. Sci. Rep. 2012, 2, 608
- Vegh, R. B. et al. Chem. Commun. 2011, 47, 4887
- Leiderman, P. et al. Chem. Phys. Lett. 2008, 455, 303
- Leiderman, P. et al. Biochemistry 2007, 46, 12026
- Stavrov, S. S. et al. J. Am. Chem. Soc. 2006, 128, 1540
- Leiderman, P. et al. J. Phys. Chem. B 2004, 108, 8043
См. также: Общий семинар ИБХ.
29 июня 2014 года

