Достижения ГНЦ ИБХ РАН
Ежегодно в ГНЦ ИБХ РАН публикуется более 500 научных статей в российских и международных рецензируемых журналах. Такое большое количество работ даёт повод представить отдельные статьи или серии статей в виде достижений ГНЦ ИБХ РАН. Каждая лаборатория один раз в год представляет свои достижения: 2010, 2011, 2012, 2013, 2014, 2015, 2016, 2017, 2018, 2019, 2020, 2021, 2022, 2023, 2024.
Кроме того, после представления всех достижений, на ученом совете выбрираются несколько особо важных, прорывных исследований, которые представляются в РАН. Ниже представлены ключевые достижения ИБХ РАН за 2020-2023 год.
2023 год
Отдел геномики адаптивного иммунитета (Чудаков Д.М.)
,Лаборатория методов иммуносеквенирования (Чудаков Д.М.)
,Лаборатория сравнительной и функциональной геномики (Лебедев Ю.Б.)
,Группа структурной организации Т-клеточного иммунитета (Британова О.В.)
Направленная деплеция TRBV9+ Т-клеток как иммунотерапия анкилозирующего спондилита
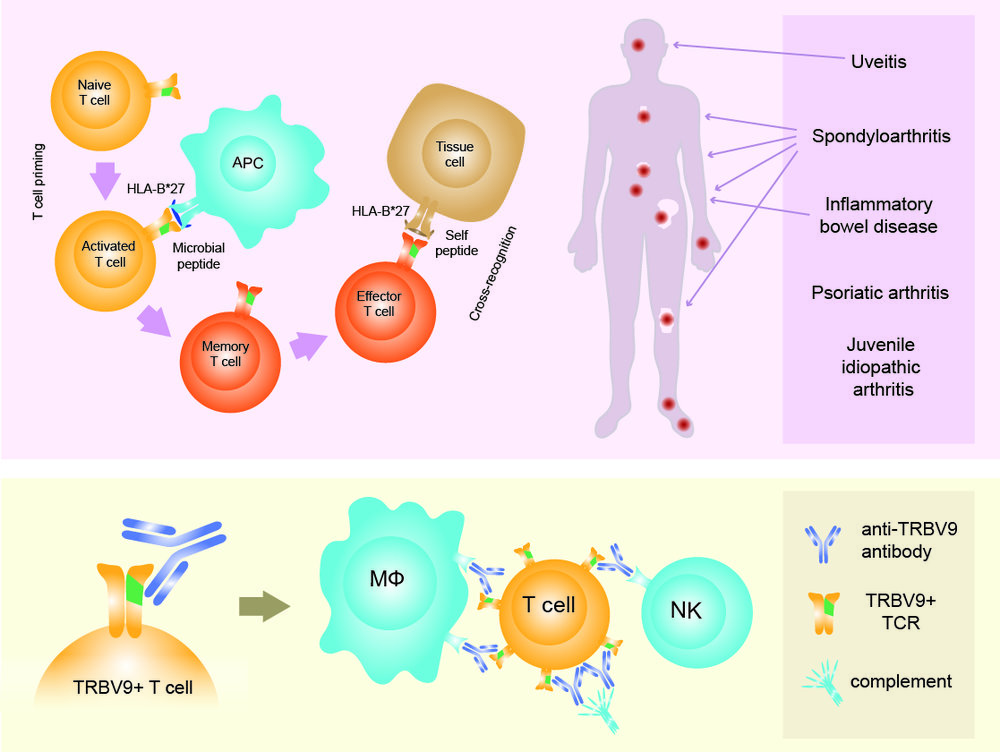
В предыдущих работах, мы идентифицировали TRBV9-содержащий мотив Т-клеточных рецепторов, ассоциированный с патогенезом анкилозирующего спондилита, псориатического артрита и острого увеита, а также HLA-B*27-презентированные бактериальные и селф-эпитопы. Здесь мы описываем доклинические испытания цитотоксических антител против TRBV9 на моделях приматов. Мы также описываем первую в мире анти-TRBV9 терапию анкилозирующего спондилита (болезни Бехтерева). Пациент достиг ремиссии в течение 3 месяцев и прекратил терапию анти-ФНО после 5 лет непрерывного применения. Полная ремиссия сохраняется в течение 4 лет, при этом ежегодно вводятся три дозы анти-TRBV9. Мы также наблюдаем значительное улучшение показателей индекса подвижности (BASMI). Описанный случай представляет собой первую в истории терапию аутоиммунного заболевания путем избирательной деплеции TRBV-подгруппы Т-лифмоцитов. Терапия анти-TRBV9 потенциально может быть применима при других спондилоартропатиях, ассоциированных HLA-B*27. В целом, такое таргетированное устранение основной причины заболевания без системной иммуносупрессии может представлять собой новое поколение безопасных и эффективных методов лечения аутоиммунных заболеваний.
- 2023 Targeted depletion of TRBV9+ T cells as immunotherapy in a patient with ankylosing spondylitis. Nat Med
Лаборатория биокатализа (Габибов А.Г.)
Показана принципиальная возможность регулировать фармакокинетику и фармакодинамику таргетных противораковых препаратов на основе ре-инжиниринга Т клеток пациента с помощью каталитических химерных антигенных рецепторов( catalytic CAR-T)
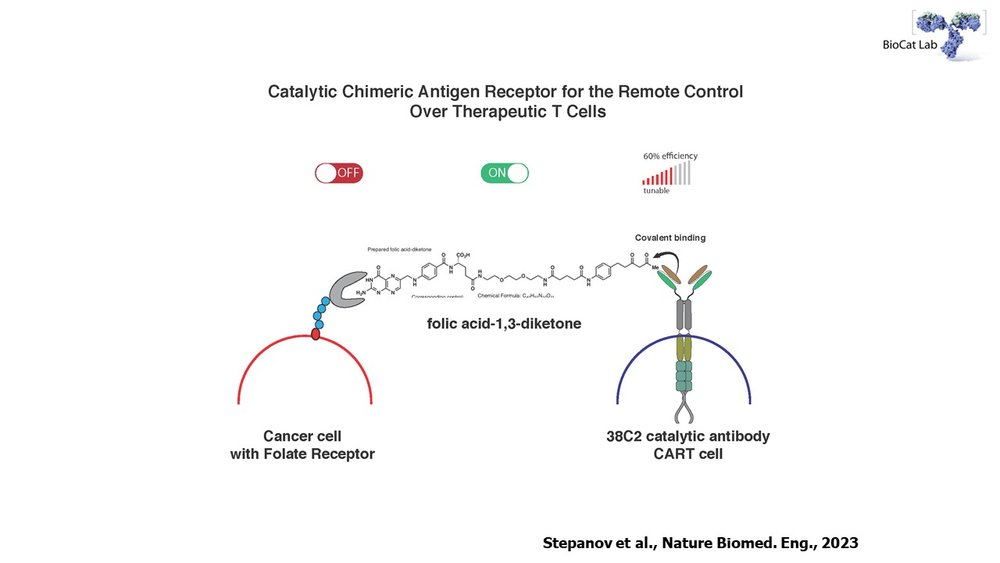
Применение модифицированных-Т клеток пациента, несущих химерный антигенный рецептор (CAR) получило широкое распространение. Однако данный революционный подход имеет существенные ограничения из-за возможности возникновения цитокинового шторма. Имеется настоятельная потребность обеспечить отмену эффекта CAR -Т в случае нежелательной реакции. Мы показывали, что специфичность и активность Т-клеток, направленных на опухоль, с CAR, состоящим из антитела с остатком лизина, который каталитически образует обратимую ковалентную связь с гаптеном 1,3-дикетона, может регулироваться концентрацией низкомолекулярных адапторов, субстратов каталитического CAR – Т. Этот адаптер избирательно связывается с гаптеном и выбранным опухолевым антигеном через низкомолекулярный связыватель, идентифицированный с помощью библиотеки, кодируемой ДНК. Таким образом, адаптер контролирует образование ковалентной связи между каталитическим антителом и гаптеном, а также привязку CAR Т-клеток к опухолевым клеткам и, следовательно, цитотоксичность и специфичность цитотоксических Т-клеток, как мы показываем in vitro. и у мышей с ксенотрансплантатами рака простаты. Такие низкомолекулярные переключения цитотоксичности и специфичности Т-клеток посредством антиген-независимого «универсального» CAR могут улучшить контроль и профиль безопасности клеточной иммунотерапии на основе CAR.
- 2023 Control of the antitumour activity and specificity of CAR T cells via organic adapters covalently tethering the CAR to tumour cells. Nat Biomed Eng
Лаборатория биомолекулярной ЯМР-спектроскопии (Бочаров Э.В.)
Нейротрофиновый рецептор TrkB как мишень для антидепрессантов нового поколения
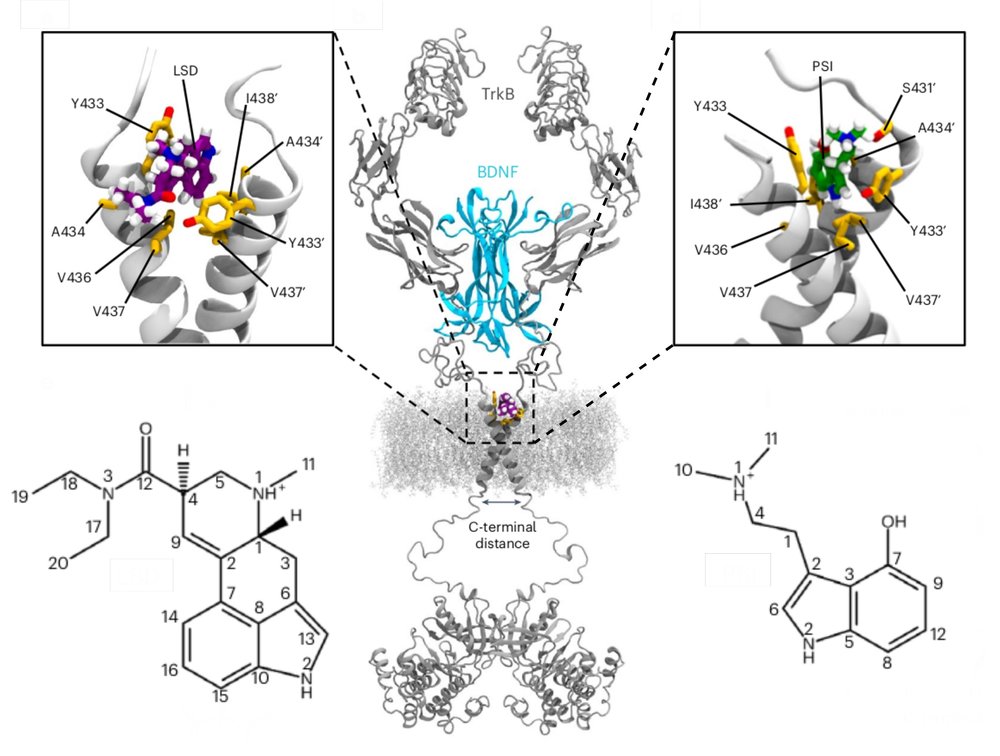
Депрессия - одна из актуальных проблем современности. Все больше исследователей утверждают, что депрессия обусловлена нарушением сигнализации нейротрофина BDNF, а его рецептор TrkB является дополнительной мишенью для целого ряда известных антидепрессантов. В ходе данной работы было установлено, что некоторые психоактивные вещества, которые очень эффективны в качестве антидепрессантов, также взаимодействуют с этим рецептором, причем с гораздо большим сродством. Однако, такие вещества обладают побочными эффектами (галлюцинации, изменение восприятия и др.) за счет связывания с другими нейрональными рецепторами. Таким образом, полученные данные дают основу для создания новых высокоэффективных антидепрессантов на основе описанных веществ, у которых будут исключены нежелательные проявления.
- 2023 Psychedelics promote plasticity by directly binding to BDNF receptor TrkB. Nat Neurosci 26 (6) 1032–1041
Лаборатория биомолекулярной ЯМР-спектроскопии (Бочаров Э.В.)
,Лаборатория моделирования биомолекулярных систем (Ефремов Р.Г.)
Примембранный цитоплазматический регион толл-подобных рецепторов - функционально-значимый элемент структуры
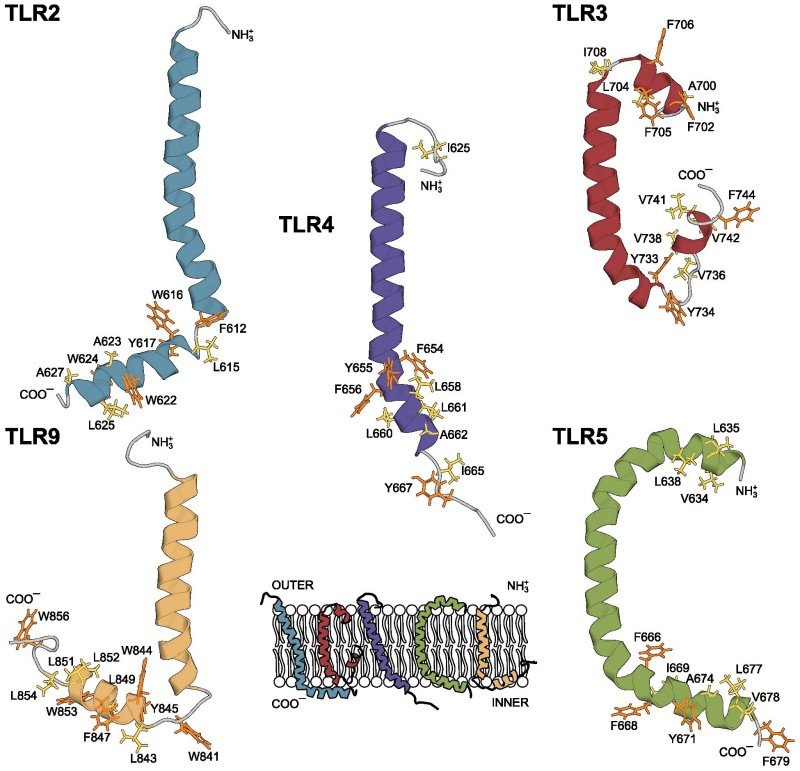
Толл-подобные рецепторы – ключевые участники врожденного иммунного ответа. Полного понимания механизмов работы TLR до сих пор нет. Это касается и структурной биологии TLR: эти рецепторы получается исследовать лишь в виде отдельных фрагментов, и не для каждой части белка есть необходимая информация, что в конечном счете не позволяет восстановить по кусочкам структуру полноразмерного TLR. Основываясь на данных ЯМР-спектроскопии были получены структуры трансмембранных и примембранных регионов. Оказалось, что примембранные регионы образуют ɑ-спираль, которая глубоко погружена внутрь мембраны, что также подтвердилось при компьютерном моделировании полученных структур. Функциональные исследования на клетках, выполненные коллегами из Китайской академии наук, совместно с данными биоинформатического анализа, позволили установить, что в данных регионах “закодированы” важные взаимодействия, необходимые для работы всего комплекса. Таким образом, примембранные участки являются активными участниками передачи сигнала.
- 2023 The architecture of transmembrane and cytoplasmic juxtamembrane regions of Toll-like receptors. Nat Commun 14 (1) 1503
Лаборатория внесинаптической передачи (Семьянов А.В.)
,Лаборатория структурной биологии ионных каналов (Шенкарёв З.О.)
,Лаборатория биоинженерии нейромодуляторов и нейрорецепторов (Люкманова Е.Н.)
,Группа клеточной пластичности мозга (Попов А.В.)
,Группа нейрон-глиальной динамики (Браже А.Р.)
,Группа редокс-нейробиологии (Браже Н.А.)
Возрастные изменения в коре головного мозга человека приводят к изменению функций митохондрий и атрофии астроцитов
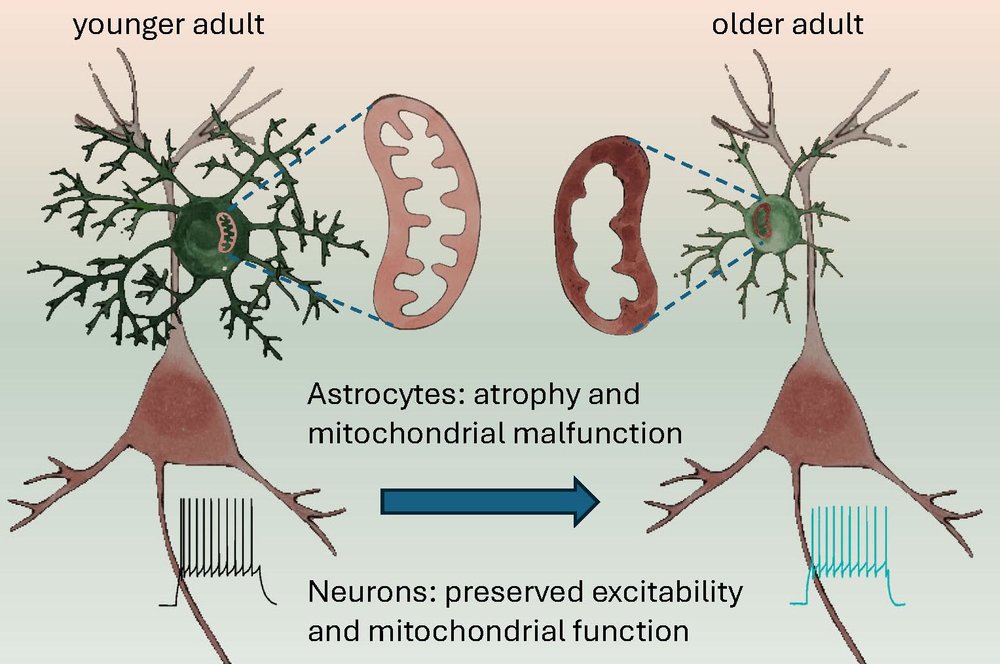
В данном исследовании были изучены сложные клеточные изменения, происходящие с возрастом в головном мозге человека. Исследование проводилось на ткани коры головного мозга человека в возрасте от 22 до 72 лет, и дало уникальную информацию о влиянии старения на астроциты и нейроны человека.
С возрастом происходит значительное снижение количества восстановленных цитохромов в астроцитах, что говорит об изменениях функций митохондрий. Примечательно, что в нейронах такого явления не наблюдалось, что подчеркивает клеточную специфичность процесса старения. Исследование выявляет изменения в соотношении белков и липидов в астроцитах и нейронах, подчеркивая сложность клеточных изменений, связанных со старением.
С возрастом также происходит атрофия астроцитов уменьшается количество их веточек, снижается объемная доля листочков, сокращается астроцитарный домен. Эти изменения коррелируют с функциональными изменениями, включающими в себя потерю связи между астроцитами через щелевые контакты и повышение входного сопротивления данных клеток.
Морфологические изменения коррелируют с увеличением количества глиального фибриллярного кислого белка (GFAP), и уменьшением эзрина, белка расположенного в астроцитарных листочках. Удивительно, но эти изменения в астроцитах не сопровождались значительными изменениями возбудимости нейронов или спонтанной тормозной постсинаптической передачи сигналов.
Представленное исследование уникально еще и потому, что результаты получены на клетках мозга человека, а не на животных. Полученные данные открывают путь к более глубокому пониманию процесса старения, учитывая реакции, специфичные для каждого типа клеток в активной среде мозга.
- 2023 Mitochondrial malfunction and atrophy of astrocytes in the aged human cerebral cortex. Nat Commun 14 (14) 8380
Лаборатория моделирования биомолекулярных систем (Ефремов Р.Г.)
Структурный механизм ингибирования онкоканала TRPV6 природными малыми молекулами
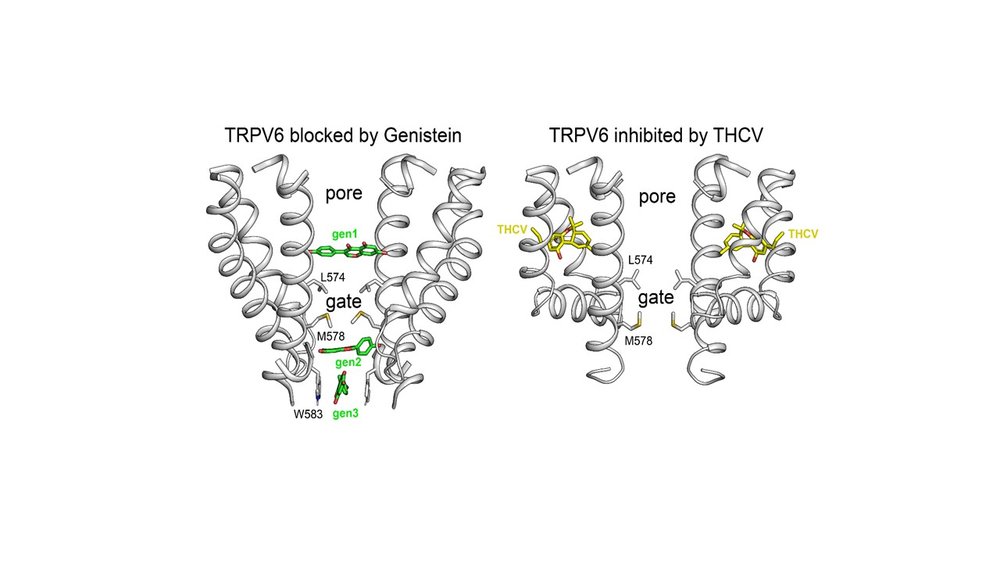
Кальций-селективный ионный канал TRPV6 является ключевым участником клеточной пролиферации, его избыточная экспрессия наблюдается при самых тяжелых видах рака у человека. Несмотря на свою фармакологическую ценность, блокаторы TRPV6 природного происхождения до сих пор не изучали. В работе выявлены структурные аспекты взаимодействия TRPV6 с природными малыми молекулами-ингибиторами: фитоэстрогеном генистеин (gen) и фитоканнабиноидом тетрагидроканнабиварин (THCV). Путем совместного применения экспериментальных и вычислительных методов показано, что gen, связываясь с TRPV6, работает как поровый блокатор, изменяющий структуру проводящей поры канала. Тогда как THCV не блокирует пору, а действует как аллостерический ингибитор, связываясь с TRPV6 в порталах, соединяющих пору с мембранным окружением. На основании данных молекулярного моделирования предложен наиболее вероятный путь связывания THCV c TRPV6. Описанные молекулярные механизмы открывают новые возможности в разработке противораковых препаратов.
Работа выполнена в сотрудничестве с лаб. А. Соболевского (Колумбийский университет, Нью-Йорк, США)
- 2023 Molecular pathway and structural mechanism of human oncochannel TRPV6 inhibition by the phytocannabinoid tetrahydrocannabivarin. Nat Commun 14 (1) 4630
- 2023 Structural mechanism of human oncochannel TRPV6 inhibition by the natural phytoestrogen genistein. Nat Commun 14 (1) 2659
2022 год
Отдел «Учебно-научный центр» (Овчинникова Т.В.)
Bet v 1-независимая сенсибилизация иммунной системы человека аллергеном пыльцы ольхи Aln g 1

Аллергия на пыльцу деревьев отряда Fagales инициируется основным аллергеном пыльцы берёзы Bet v 1. Известно, что аллерген-специфические Т-клетки играют ключевую роль в процессе сенсибилизации иммунной системы. Совместно с коллегами из Венского медицинского университета впервые было проведено картирование Т-клеточных эпитопов Aln g 1 (1А), проведена оценка пролиферации Т-клеток (1Б), ингибирование связывания специфических IgE из сывороток пациентов с аллергией с Aln g 1 (2А) и Bet v 1 (2Б) в результате преинкубации сывороток пациентов с различными концентрациями Bet v 1 (белые ячейки) и Aln g 1 (серые ячейки), а также ответ Т-клеток пациентов на стимуляцию Bet v 1 (3А) и Aln g 1-специфичных Т-клеток на стимуляцию различными аллергенами (3Б). Полученные результаты свидетельствуют о том, что основные аллергены Fagales обладают способностью вызывать независимую от Bet v 1 сенсибилизацию у пациентов, проживающих в регионах с преобладанием берёзовых деревьев.
- 2022 Bet v 1-independent sensitization to major allergens in Fagales pollen: evidence at the T cell level. Allergy 78 (3) 743–751
Лаборатория молекулярных основ эмбриогенеза (Зарайский А.Г.)
Гены скейлеры - регуляторы масштабной инвариантности эмбрионального развития
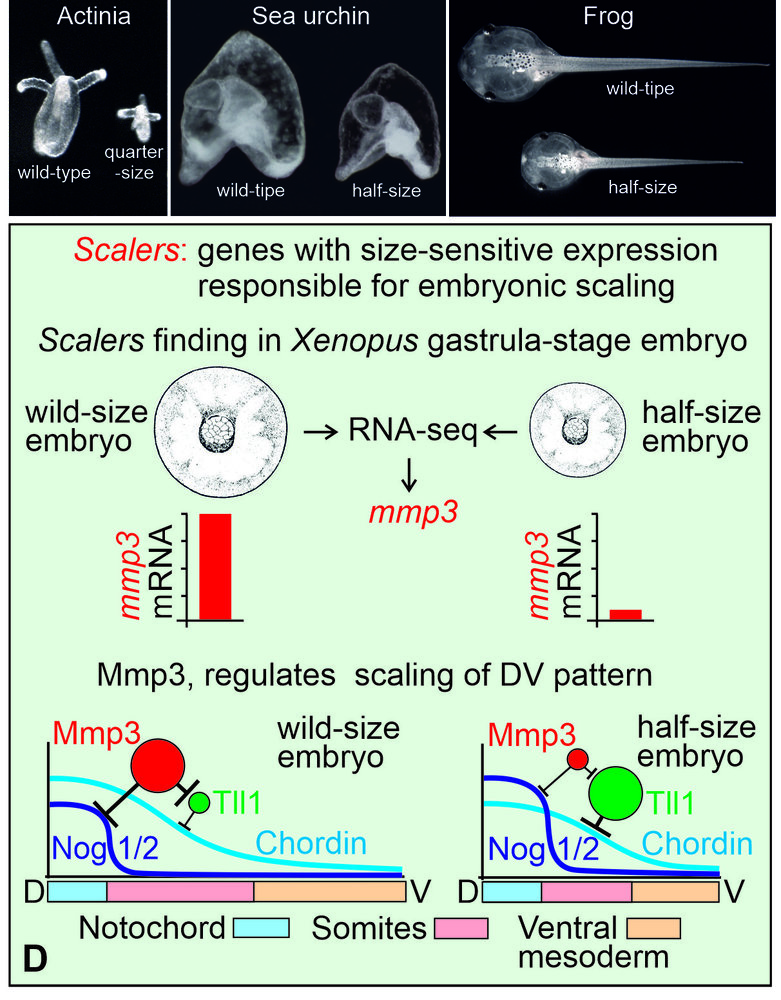
Эмбрионы многих организмов способны сохранять инвариантность своей структуры, не зависимо от размера - т.н. явление эмбрионального скейлинга (от анг. scale – масштаб). Например, эмбрионы морского ежа или лягушки, развившиеся из отдельных клеток, изолированных вскоре после начала дробления яйца, регулируют свою структуру так, что выглядят как уменьшенные копии нормальных. Этот феномен, известный уже более 100 лет, является наиболее ярким проявлением фундаментального, но все еще плохо изученного, свойства живых организмов использовать на систематической основе неравновесную самоорганизацию для своего структурирования. Мы впервые предсказали и математически доказали существование специальных генов-скейлеров, играющих роль размерных сенсоров благодаря зависимости их экспрессии от размеров эмбрионов. Также мы разработали метод прицельного поиска скейлеров и описали на примере одного из них, гена матриксной металлопротеиназы 3 (Mmp3), не известный ранее механизм размер- зависимой регуляции эмбрионального паттернинга у шпорцевой лягушки.
- 2022 Targeted search for scaling genes reveals matrix metalloproteinase 3 as a scaler of the dorsal-ventral pattern in Xenopus laevis embryos. Dev Cell 57 (1) 95–111.e12
Лаборатория молекулярной иммунологии (Деев С.М.)
,Лаборатория онконанотераностики (Звягин А.В.)
Мгновенное высвобождение лекарства из наночастиц, накопившихся в ближайших к опухоли сосудах, многократно усиливает терапевтический эффект
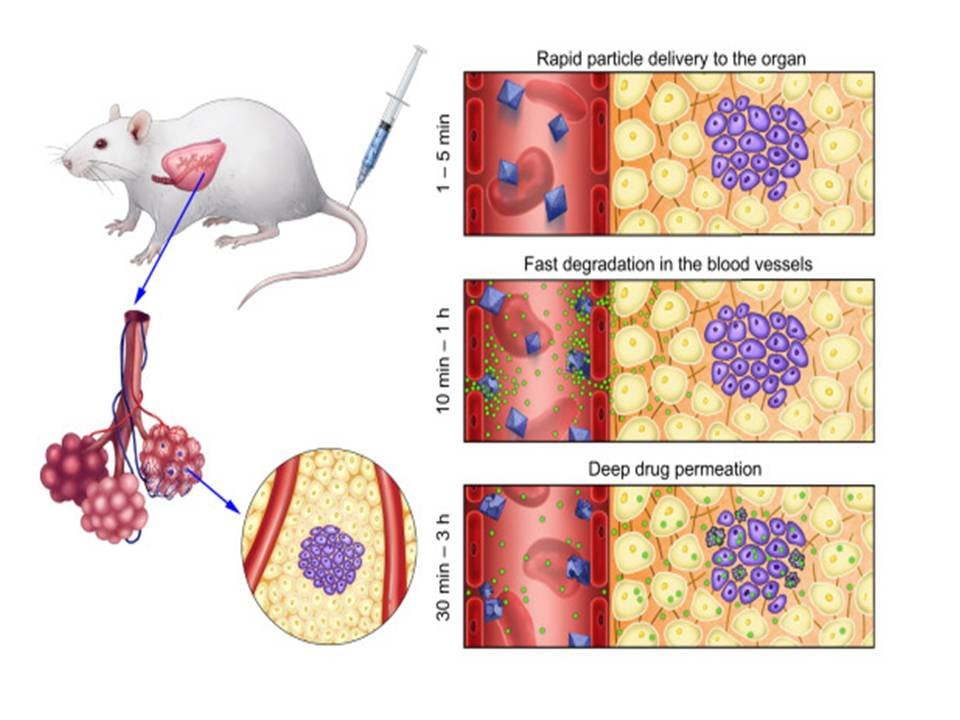
Разработан принципиально новый подход доставки лекарств, основанный не на EPR-эффекте, а на быстром разрушении в кровотоке наноконтейнеров, нагруженных химиопрепаратом. Метод включает экстравазацию не наночастиц, а лекарства из сосуда в интерстиций, и далее в паренхиму опухоли. Эффективность подхода, продемонстрированная in vivo на модели ранних метастазов меланомы в легких, на порядок превосходит эффективность традиционной химиотерапии.
- 2022 Flash drug release from nanoparticles accumulated in the targeted blood vessels facilitates the tumour treatment. Nat Commun 13 (1) 6910
Лаборатория микрофлюидных технологий для биомедицины (Тоневицкий А.Г.)
Изменения в презентации пептидов SARS-CoV-2 Omicron и Delta молекулами HLA
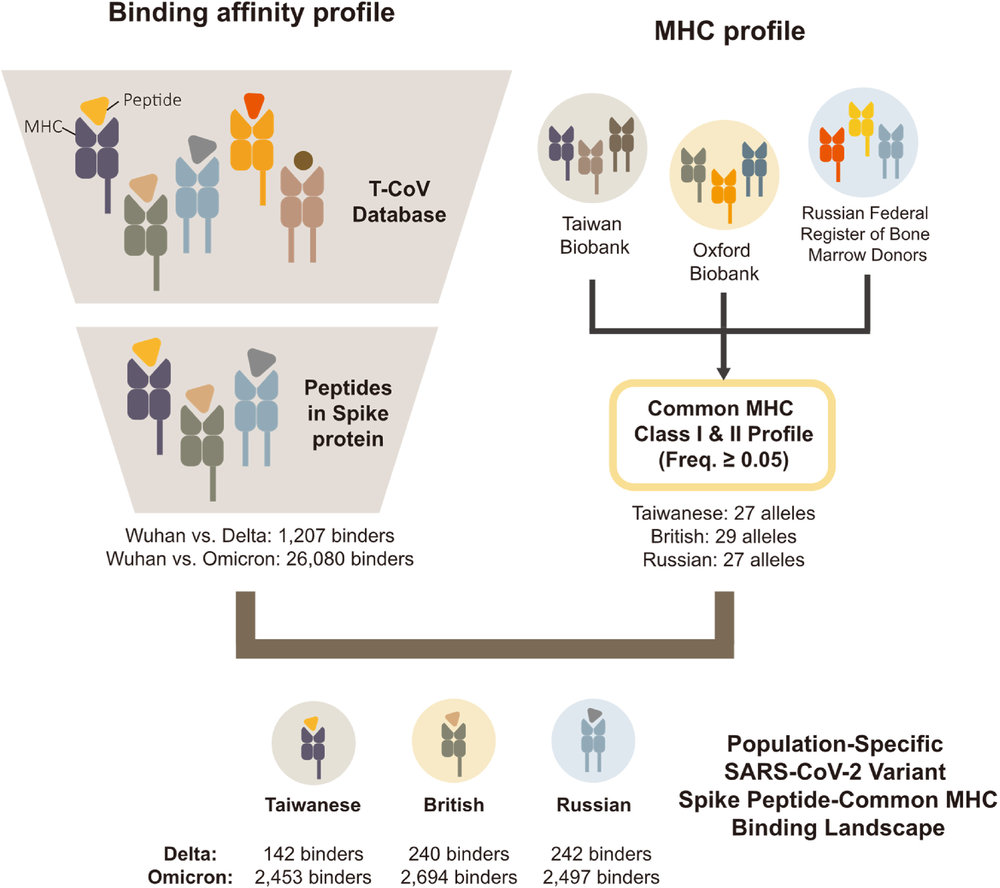
Иммунный ответ Т-клеток является основным фактором, определяющим эффективный клиренс SARS-CoV-2. Используя недавно разработанный биоинформационный портал T-CoV (https://t-cov.hse.ru), мы проанализировали особенности презентации вирусных пептидов для вариантов SARS-CoV-2 Omicron, Delta и Wuhan. Сначала мы показали отсутствие существенных различий в презентации пептидов, полученных из SARS-CoV-2, наиболее часто встречающимися аллелями HLA класса I/II и соответствующими гаплотипами HLA. Затем анализ был ограничен набором пептидов, происходящих из S-белков рассматриваемых вариантов SARS-CoV-2. Главным результатом стало разрушительное воздействие мутаций Omicron на пептид PINLVRDLPQGFSAL, который был единственным сильно связывающимся пептидом S-белка для аллеля HLA-DRB1*03:01 и некоторых соответствующих гаплотипов. В частности, мы предсказали резкое снижение аффинности связывания HLA-DRB1*03:01 и этого пептида как из-за мутаций Omicron BA.1 (делеция N211, замена L212I и вставка EPE 212-214), так и из-за мутаций Omicron BA.2 (замена V213G). Биоинформатический прогноз был экспериментально подтвержден методом ИФА с использованием соответствующих тиоредоксин-связанных пептидов и рекомбинантных молекул HLA-DR. Еще одним результатом стало значительное уменьшение количества сильно связывающихся пептидов S-белка для аллеля HLA-B*07:02 HLA класса I (как для вариантов Omicron, так и Delta). В целом, на большинство аллелей и гаплотипов HLA мутации существенно не повлияли, что свидетельствует о сохранении эффективного Т-клеточного иммунитета против вариантов Omicron и Delta. Наконец, мы внесли вариант Omicron в портал T-CoV и добавили в него функцию анализа на уровне гаплотипов.
Были исследованы изменения профилей сродства связывания S-белка с HLA между штаммом Wuhan и двумя доминантными вариантами, штаммами Delta и Omicron, среди тайваньской, британской и российской популяций.
Для штамма Delta сильное связывание измененных пептидов с аллелями HLA снижается во всех трех популяциях и почти исчезает в тайваньской популяции. Для штамма Omicron сильные связи в основном сохраняются для обоих классов HLA и в тайваньской и британской популяциях, с небольшим снижением HLA класса II в тайваньской (1,4%), в то время как в российской популяции сохраняется относительно высокая доля сильных связей для обоих классов HLA.
- 2022 On the peptide binding affinity changes in population-specific HLA repertoires to the SARS-CoV-2 variants Delta and Omicron. J Autoimmun 133 102952
- 2022 Immunogenic epitope panel for accurate detection of non-cross-reactive T cell response to SARS-CoV-2. JCI Insight 7 (9)
- 2022 Alterations in SARS-CoV-2 Omicron and Delta peptides presentation by HLA molecules. PeerJ 10 e13354
- 2021 T-CoV: a comprehensive portal of HLA-peptide interactions affected by SARS-CoV-2 mutations. Nucleic Acids Res 50 (D1) D883–D887
Лаборатория клеточных взаимодействий (Сапожников А.М.)
Разработка метода выделения экзосом с применением ассиметричной фильтрации
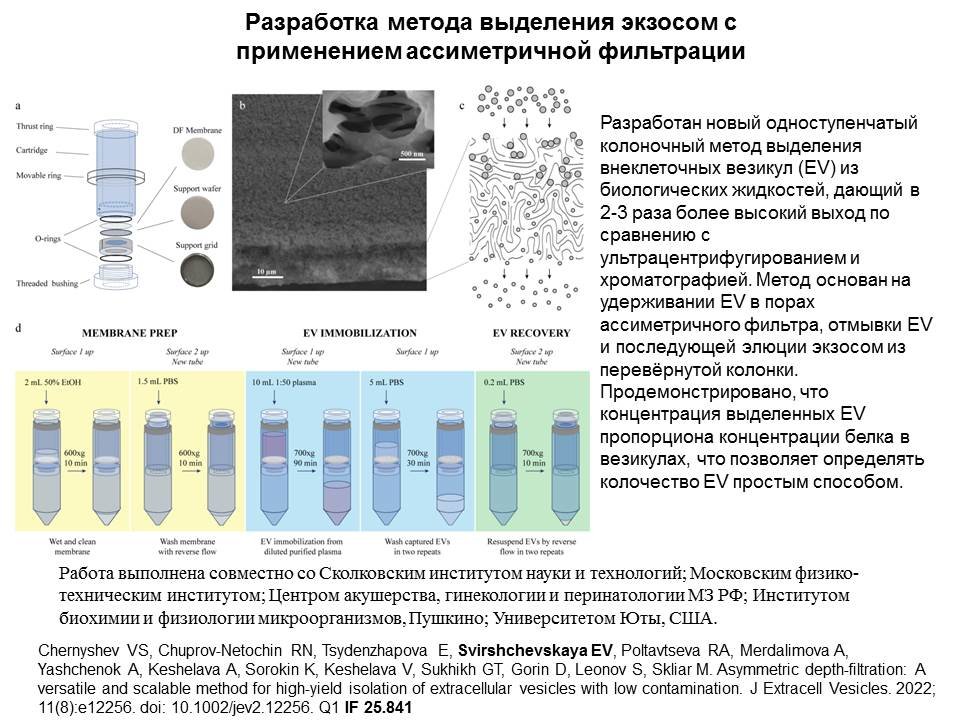
Разработан новый одноступенчатый колоночный метод выделения внеклеточных везикул (EV) из биологических жидкостей, дающий в 2-3 раза более высокий выход по сравнению с ультрацентрифугированием и хроматографией. Метод основан на удерживании EV в порах ассиметричного фильтра, отмывки EV и последующей элюции экзосом из перевёрнутой колонки. Продемонстрировано, что концентрация выделенных EV пропорциона концентрации белка в везикулах, что позволяет определять колочество EV простым способом.
- 2022 Asymmetric depth-filtration: A versatile and scalable method for high-yield isolation of extracellular vesicles with low contamination. J Extracell Vesicles 11 (8) e12256
Группа алгоритмов иммуносеквенирования (Шугай М.А.)
VDJdb в эпоху пандемии: база данных Т-клеточных рецепторов, распознающих эпитопы вируса SARS-CoV-2
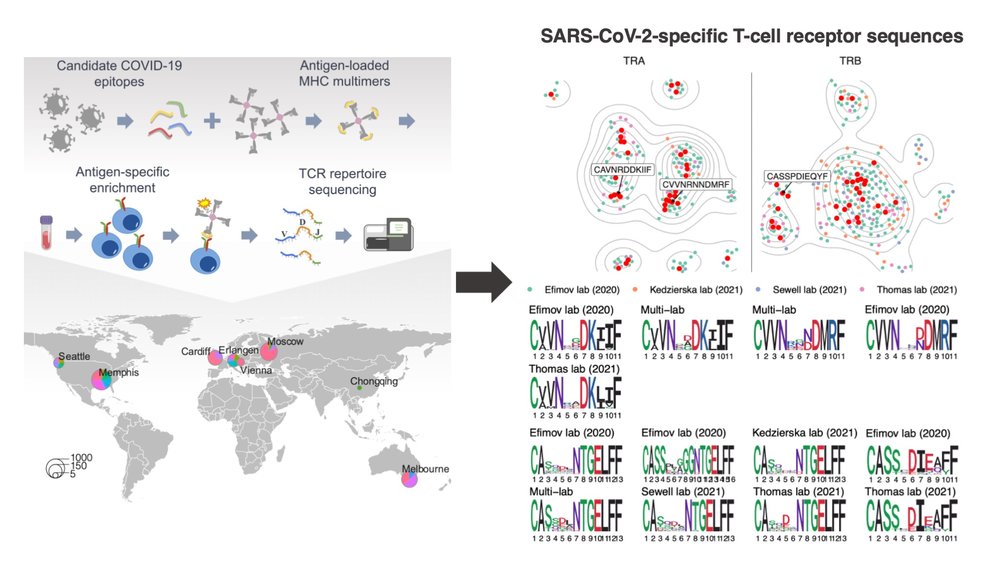
В данной работе мы описываем обновление базы данных VDJdb проведенное в период 2019-2022гг и связанное с пандемией вируса SARS-CoV-2. Это обновление включает в себя последовательности альфа- и бета-цепей Т-клеточных рецепторов, способных распознавать различные эпитопы вируса представляемые различными аллелями HLA. Кроме того, нами были выявлены характерные аминокислотные мотивы последовательностей Т-клеточных рецепторов распознающих эпитоп A*02-YLQ вируса SARS-CoV-2 и показана воспроизводимость результатов по данным анализа крови пациентов полученных в различных лабораториях расположенных по всему земному шару.
- 2022 VDJdb in the pandemic era: a compendium of T cell receptors specific for SARS-CoV-2. Nat Methods 19 (9) 1017–1019
Отдел геномики адаптивного иммунитета (Чудаков Д.М.)
Идентификация эпитопов, распознаваемых Т-клеточным рецептором, ассоциированным с анкилозирующим спондилитом.
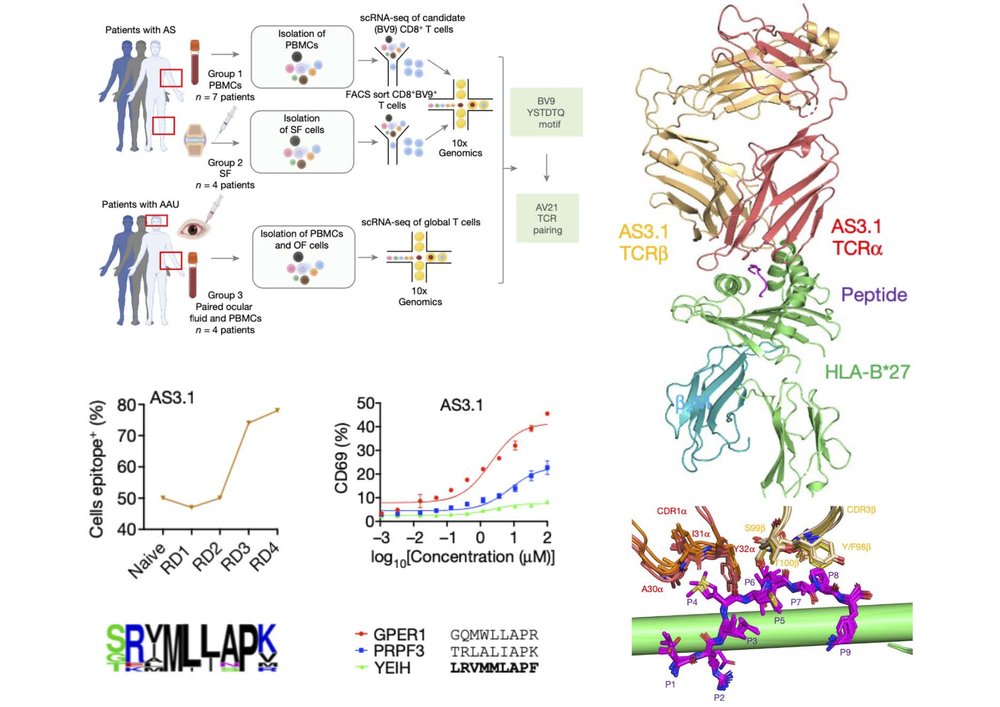
Анкилозирующий спондилоартрит (АС) – ревматологическое заболевание аутоиммунной природы. В основе развития аутоиммунных патологий лежит реализация иммунного ответа организма против антигенов собственных клеток. Идентификация антигенов, распознаваемых рецепторами Т-лимфоцитов, в особенности аутоантигенов, на данный момент представляет технологически весьма сложную задачу. К настоящему времени удалось охарактеризовать антигенную специфичность буквально лишь нескольких таких Т-клеточных рецепторов (TCR). При этом получаемые сведения совершенно необходимы как для понимания общих правил распознавания Т-клетками специфических антигенов, так и для понимания механизма развития аутоиммунного заболевания и разработки терапевтических подходов подобных состояний.
В лаборатории Сравнительной и функциональной геномики отдела Геномики адаптивного иммунитета ИБХ удалось установить полную последовательность для TCR, ассоциированного с анкилозирующим спондилоартритом. Совместно с коллегами из университетов Стэнфорда, Оксфорда и университета Дж. Вашингтона в Сент-Луисе, удалось расширить группу АС-ассоциированных TCR с известной последовательностью и определить узнаваемые ими Т-клеточные эпитопы (антигены). С помощью рентгеноструктурного анализа нескольких комплексов ТCR с соответствующими комплексами пептид-МНС удалось определить ключевые аминокислотные остатки, определяющие узнавание антигенных пептидов. Были найдены распознаваемые этими TCR антигенные пептиды из белков организма человека и ряда кишечных бактерий.
Полученные результаты поддерживают гипотезу кросс-реактивности Т-клеток при узнавании микробных антигенов и антигенов клеток собственного организма как механизма запуска аутоиммунной реакции при АС. Знание структуры антигенов, распознаваемых АС-ассоциированными TCR открывает широкие возможности для изучения механизма участия этой группы Т-клеток в патогенезе заболевания и развития принципиально новых подходов к терапии анкилозирующего спондилита.
- 2022 Autoimmunity-associated T cell receptors recognize HLA-B*27-bound peptides. Nature 612 (7941) 771–777
Лаборатория молекулярной иммунологии (Деев С.М.)
,Группа экспрессии белковых факторов роста и дифференцировки (Фролова Е.И.)
,НПП «Питомник лабораторных животных» (Телегин Г.Б.)
Генетически кодируемая система, основанная на биолюминесцентном резонансном переносе энергии, для фотодинамической терапии глубинных опухолей
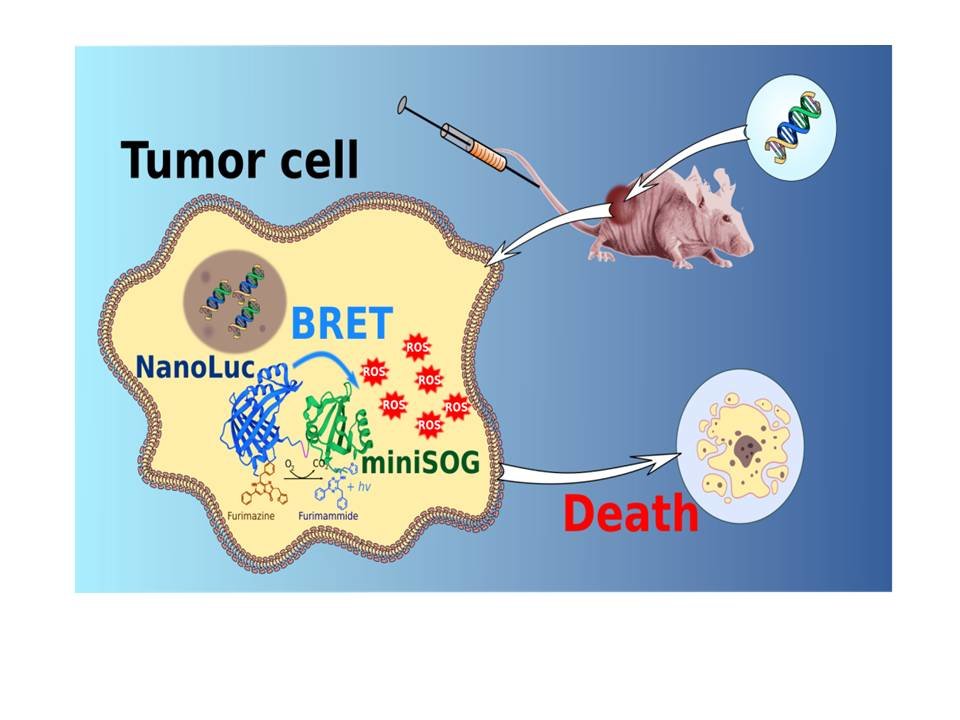
Разработана генетически-кодируемая система для фотодинамической терапии на основе биолюминесцентного резонансного переноса энергии (BRET). Данная система содержит так называемый «внутренний» источник света (люциферазу NanoLuc) и фотосенсибилизатор (фототоксичный белок miniSOG). NanoLuc-miniSOG представляют собой BRET-пару, в которой окисленная форма люциферазного субстрата является донором энергии для возбуждения miniSOG, который, в свою очередь, генерирует АФК. Будучи генетически кодируемой, данная конструкция может быть доставлена к опухолям, расположенным практически на неограниченной глубине. Используя псевдотипированные лентивирусы, специфичные к опухоль-ассоциированному антигену, была продемонстрирована адресная доставка созданной генетической конструкции непосредственно в опухолевые клетки in vivo и проведена ФДТ без внешнего источника света. При этом коэффициент ингибирования роста опухоли (TGI) составил более 67%. Таким образом, проведенное исследование является доказательством возможности проведения ФДТ глубинных новообразований без внешнего источника света.
- 2022 Genetically encoded BRET-activated photodynamic therapy for the treatment of deep-seated tumors. Light Sci Appl 11 (1) 38
Лаборатория молекулярной вирусологии (Рубцов Ю.П.)
,Лаборатория биокатализа (Габибов А.Г.)
SARS-CoV2 –специфические Т-клетки и антитела для защиты от коронавирусной болезни 2019 (COVID-19): проспективное исследованиеЛаборатория молекулярной вирусологии (Рубцов Ю., Мусатова О., Дерябин А.)в сотрудничестве с Лабораторией биокатализа (Ломакин Я.,
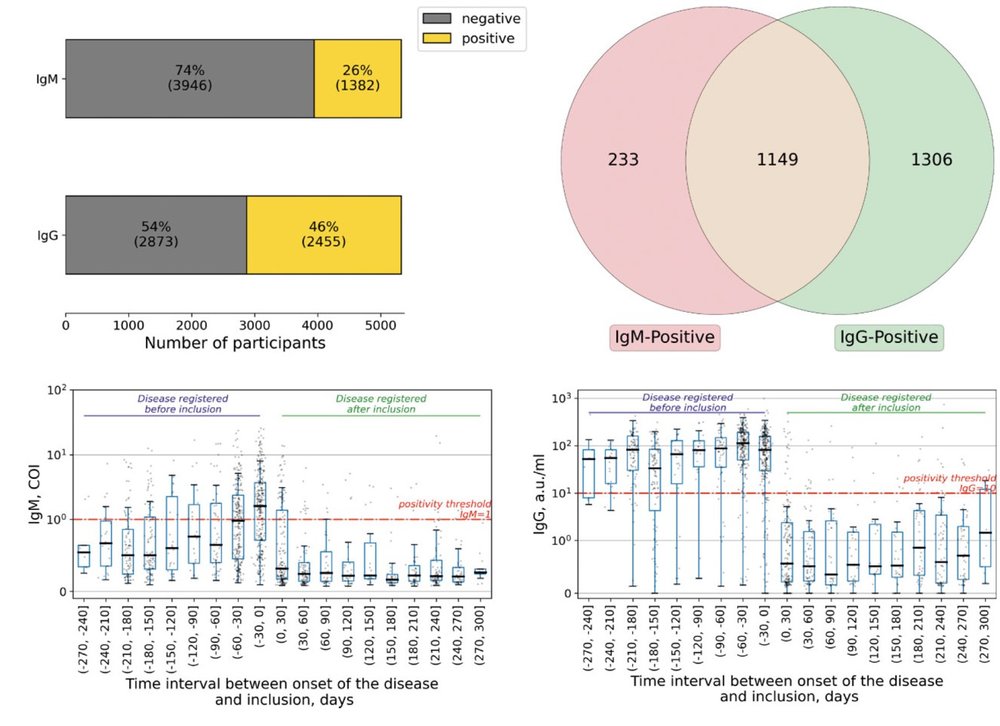
Исследование было сосредоточено на вопросе: есть ли специфические антитела против белков SARS-CoV2 и соответствующие антиген-специфические Т-клетки у здоровых доноров, и достаточно ли их для защиты от инфекции и заболевания COVID-19?
5400 здоровых доноров города Москвы были протестированы на IgG и IgM к белкам SARS-CoV-2. Значительная часть неинфицированных доноров имела значительный уровень анти-SARS-CoV2 Ig, а также вирусспецифические Т-клетки, продуцирующие IFN-g и IL-2. Величина ответов обратно пропорциональна вероятности заражения, в то время как уровень иммуноглобулина оказывал более выраженное влияние на защиту, чем ответ Т-клеток.
Данные о титрах вирусспецифических IgG могут быть информативными для принятия решений по сопосбам борьбы с COVID-19.
- 2022 SARS-CoV-2-specific T cells and antibodies in COVID-19 protection: a prospective study. Clin Infect Dis 75 (1) e1–e9
Лаборатория биокатализа (Габибов А.Г.)
,Лаборатория молекулярной иммунологии (Деев С.М.)
Универсальные модульные CAR на основе взаимодействия барназы с барстаром. Модуль направляет на опухолевый антиген дарпин, слитый с барназой, барстар входит в состав CAR (BsCAR).
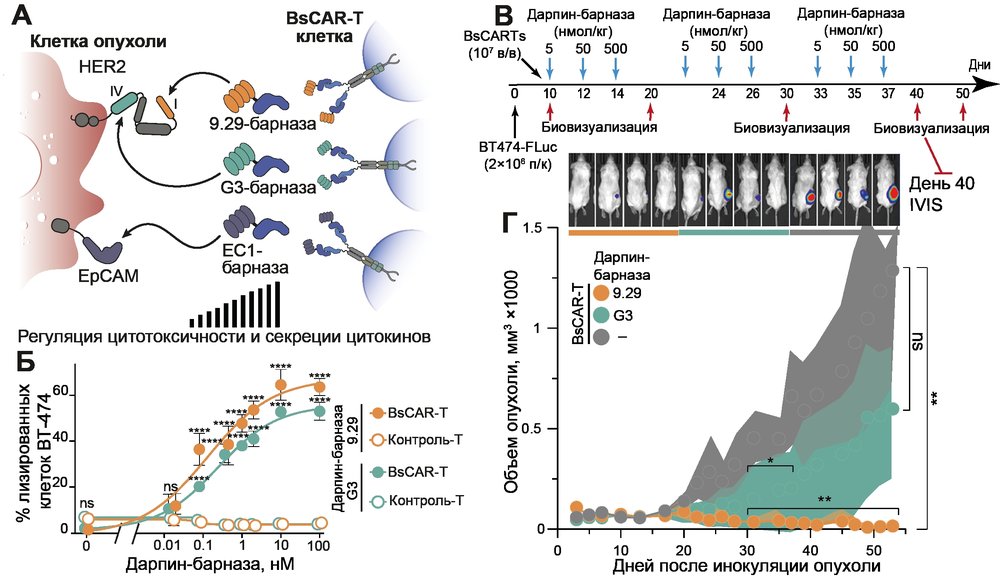
А) За счет модульности можно менять нацеливание CAR-T клеток на разные части антигена, а также на другие ассоциированные с опухолью антигены. Изменяя концентрацию молекул-посредников происходит контроль активности CAR-T клеток. Что позволит преодолеть опасности сопряженные с терапией CAR-T клетками (гиперцитокинемия (цитокиновый шторм), синдром лизиса опухоли).
Б) подтверждение регуляции активности in vitro (цитотоксический тест на клетки с гиперэкспрессией HER2, с двумя видами молекул-посредников 9.29-барназа и G3-барназа.
В,Г) подтверждение работоспособности системы in vivo. В) схема эксперимента на мышах. Вводим молекулы-посредники циклами с повышением дозы, что способствует лучшей персистенции CAR-T клеток, а также предотвращает гиперактивацию CAR-T. Репрезентативные фотографии мышей на IVIS на 40 день после прививания опухоли, всем мышам вводили CAR-T клетки, 1 группе вводили 9.29-барназу, второй G3-барназу (проксимальная часть HER2), в контрольной группе вводили PBS. Г) Объем опухоли измеренный штангенциркулем. 9.29-барназа сработала лучше в мышах, так как антиген на который нацелен 9.29 дарпин на дистальной части HER2.
2021 год
- 2022 Switchable targeting of solid tumors by BsCAR T cells. Proc Natl Acad Sci U S A 119 (46) e2210562119
Лаборатория биокатализа (Габибов А.Г.)
,Отдел пептидно-белковых технологий (Тоневицкий А.Г.)
,Лаборатория молекулярной иммунологии (Деев С.М.)
,НПП «Питомник лабораторных животных» (Телегин Г.Б.)
Антиген-специфичная стимуляция и экспансия CAR-T клеток с использованием искусственных везикул.
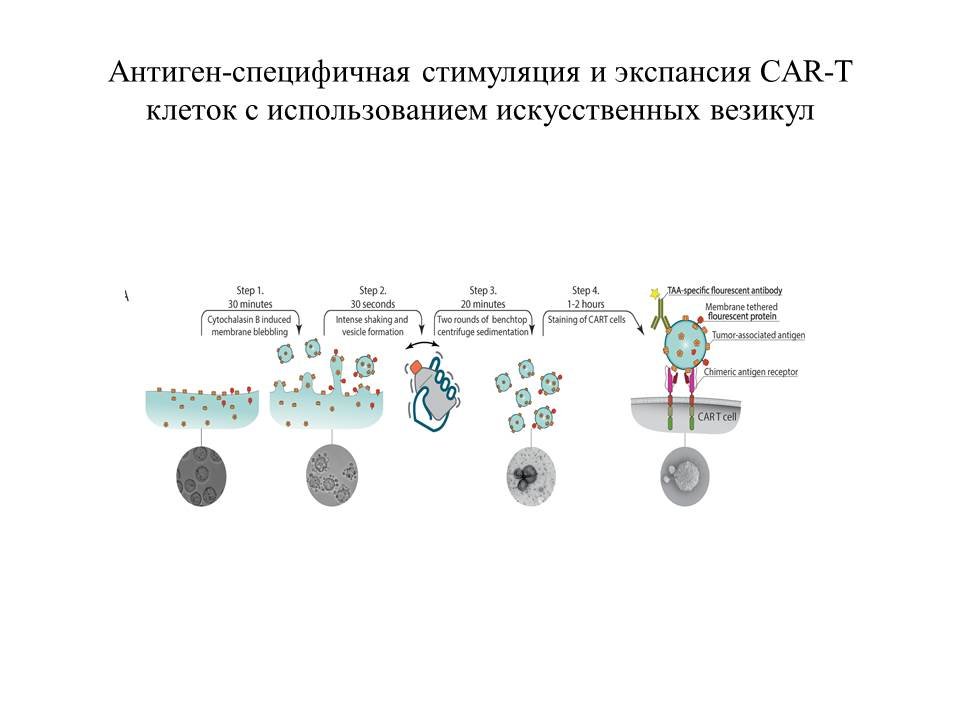
Инженерия Т-клеток человека сделала революцию в онкологии. Разработка CAR-T терапии привела к значительному успеху в лечении В-клеточного лейкоза. Критическим этапом технологии является наработка in vitro из донорских аутологичных Т клеток CAR-T с заранее заданной антигенной специфичностью. Для разработки специфического улучшенного протокола экспансии CAR-T-клеток предложено использовать клеточные мембранные везикулы стабильно экспрессирующие поверхностно-связанные антигены CAR. В опытах in vivo продемонстрировано что антиген-специфические везикулы способны вызывать более сильную стимуляцию, пролиферацию и функциональную активность CAR-T-клеток. Новая методология значительно расширит возможности получения улучшенных популяций функциональных CAR-T-клеток для терапии рака.
- 2021 Antigen-Specific Stimulation and Expansion of CAR-T Cells Using Membrane Vesicles as Target Cell Surrogates. Small 17 (45) e2102643
Лаборатория белков гормональной регуляции (Белогуров А.А.)
,Группа химии гетероциклических соединений (Баранов М.С.)
Глубинное профилирование метаболизма убиквитина в клетках млекопитающих с применением флуоресцентного трекинга
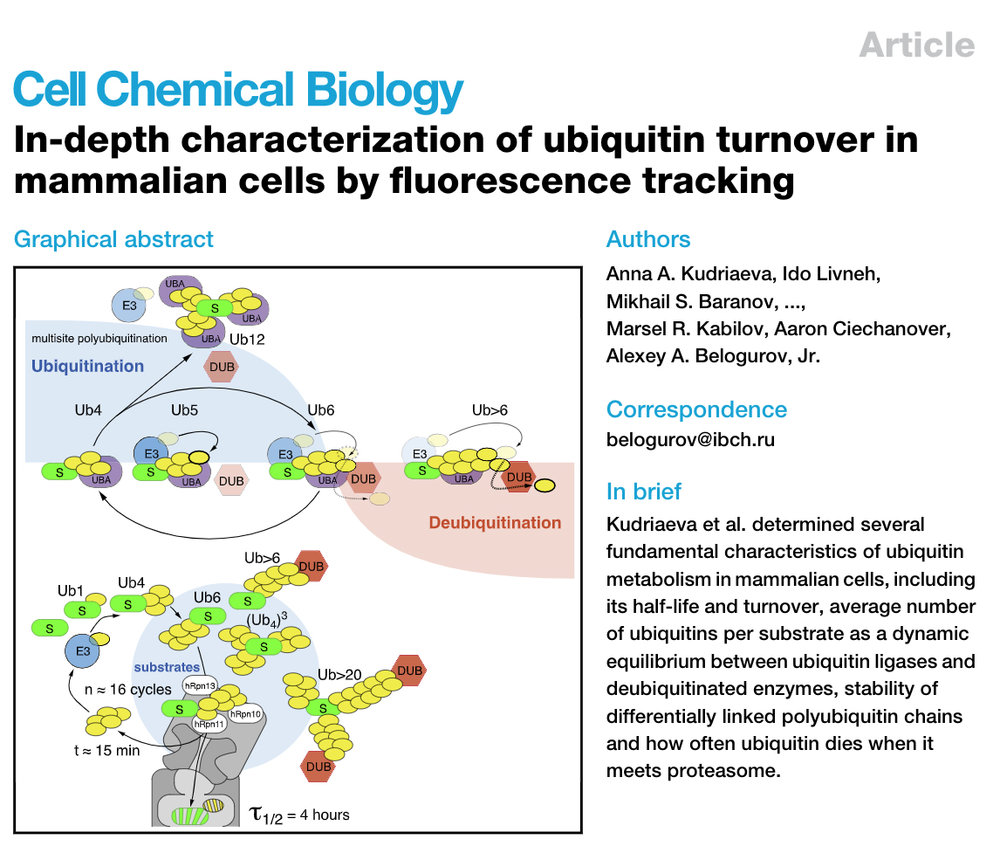
Определено время полужизни убиквитина в клетках млекопитающих (4 часа)
Показано, что усреднённо в клетке белки конъюгированы с 6 остатками убиквитина
Выявлено, что молекула убиквитина участвует в среднем в 16 циклах конъюгации, а безвозвратные потери убиквитина составляют одна молекулу на 4 акта захвата полиубиквитинированного субстрата протеасомой
Аминокислотный остаток UbK27 является критичным в терминах внутриклеточной стабильности убиквитина в целом
- 2021 In-depth characterization of ubiquitin turnover in mammalian cells by fluorescence tracking. Cell Chem Biol 28 (8) 1192–1205.e9
Лаборатория молекулярной иммунологии (Деев С.М.)
Инновационный радиофармпрепарат на основе рекомбинантного DARPin G3 для радионуклидной диагностики рака молочной железы с гиперэкспрессией HER2/neu успешно прошел I фазу клинических испытаний.
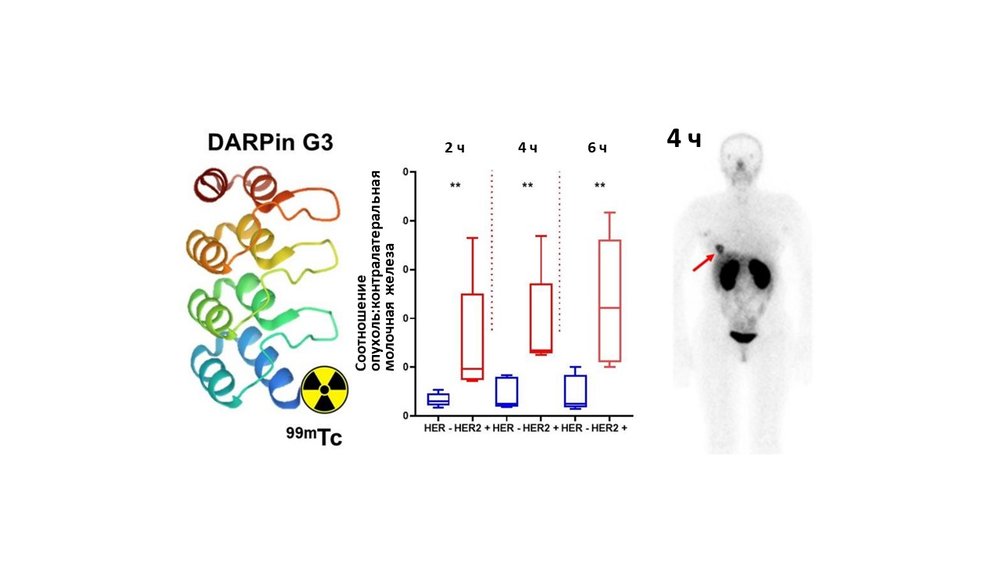
Проведена I фаза клинических испытаний инновационного радиофармпрепарата 99mTc-DARPin G3, созданного на основе меченного 99мтехнецием рекомбинантного адресного полипептида DARPin G3 и предназначенного для радионуклидной диагностики рака молочной железы с гиперэкспрессией HER2/neu. Показано, что визуализация экспрессии опухолевого маркера HER2/neu с использованием 99mTc-DARPin G3 безопасна, обеспечивает низкую дозовую нагрузку на организм и хорошо переносится пациентами. Полученные изображения опухолей позволяют достоверно различать HER2-положительный и HER2-отрицательный рак груди, позволяя врачу выбрать обоснованный протокол лечения. Успешные результаты I фазы клинических испытаний служат основанием для дальнейшей клинической разработки диагностического радиофармпрепарата 99mTc-DARPin G3.
- 2021 Phase I trial of 99mTc-(HE)3-G3, a DARPin-based probe for imaging of HER2 expression in breast cancer. J Nucl Med 63 (4) 528–535
Лаборатория биомолекулярной ЯМР-спектроскопии (Бочаров Э.В.)
,Лаборатория моделирования биомолекулярных систем (Ефремов Р.Г.)
Описан молекулярный механизм действия D3 пептидов в процессе разрушения β-амилоидных олигомеров
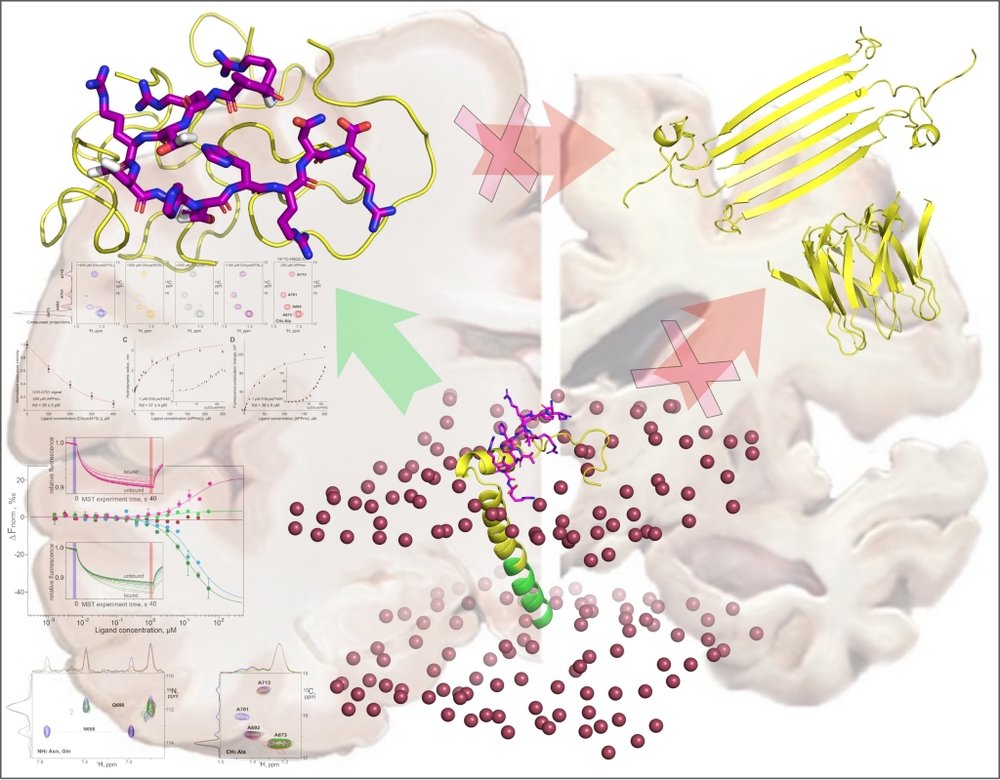
Болезнь Альцгеймера - самый распространенный в мире вид нейродегенеративного заболевания. В патогенезе болезни задействованы различные пептиды и белки, в том числе бета-амилоидный пептид (Aβ). Известно, что все изоформы Aβ склонны к ассоциации, и именно олигомеры играют решающую роль в патогенезе болезни Альцгеймера, оказывая токсическое действие на нейроны и их органеллы. Немецкими учеными был создан D-энантиомерный пептид D3, который участвует в разрушении цитотоксических малых олигомеров Aβ. В рамках работы по изучению этого белка было показано, что D3, стабилизирующий мономерный Aβ, динамически взаимодействует с прилегающей к мембране областью мембранного белка предшественника β-амилоида— трансмембранного фрагмента APP672-726 (Aβ1-55). На основе данных ЯМР и молекулярного моделирования было показано, что D3 нацелен на амилоидогенную область Aβ, тем самым ингибируя ранние стадии перехода пептида Aβ в β-конформацию, характерную для малых токсичных олигомеров. Было обнаружено, что D3 и Aβ1-55, являясь неупорядоченными белками, при взаимодействии образуют подвижный, но устойчивый комплекс, в котором конформации обоих полипептидов постоянно изменяются с изменением паттерна межмолекулярных контактов. Такие динамические межмолекулярные взаимодействия D3 пептидов лежат в основе их молекулярного механизма разрушения цитотоксических β-амилоидных олигомеров, а именно подавления контактов между Aβ пептидами и сохранения их в α-спиральной конформации, что предотвращает их переход в β-тяжи.
- 2021 All-d-Enantiomeric Peptide D3 Designed for Alzheimer’s Disease Treatment Dynamically Interacts with Membrane-Bound Amyloid-β Precursors. J Med Chem 64 (22) 16464–16479
- 2021 Structural Studies Providing Insights into Production and Conformational Behavior of Amyloid-β Peptide Associated with Alzheimer's Disease Development. Molecules 26 (10)
Лаборатория биомолекулярной ЯМР-спектроскопии (Бочаров Э.В.)
ЯМР-спектроскопия в реальном времени — методика исследования сайтов фосфорелирования Тау-белка в норме и патологии
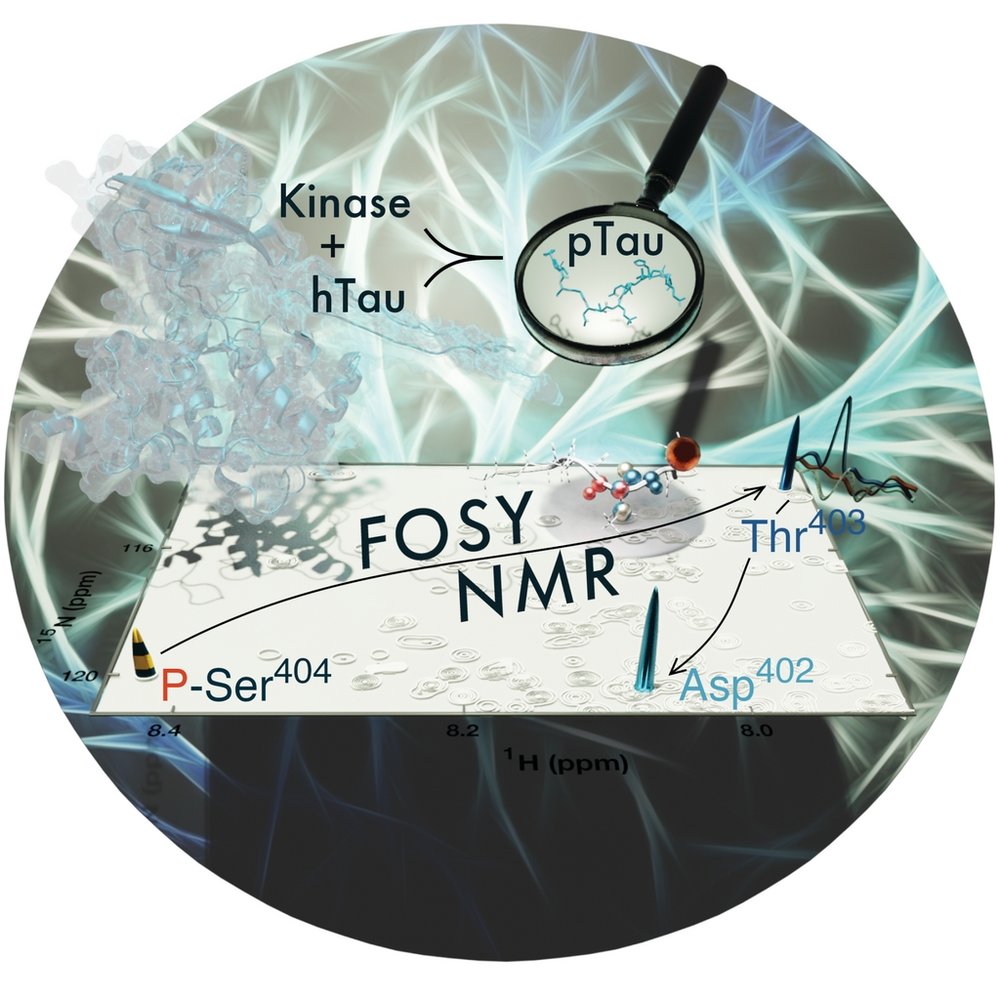
При исследовании белков, как правило, основной интерес представляют «hotspots» - их функционально-активные участки, которые ответственны за ключевые процессы в каскаде биологических реакций. Метод ЯМР-спектроскопии позволяет на атомном уровне взглянуть на эти процессы, однако, классические подходы неизменно включают стадию полного отнесения сигналов белка, что ресурсозатратно как в плане приборного, так и рабочего времени. Это зачастую является «узким местом» в драг-дизайн и существенным сдерживающим фактором для выполнения проекта в кратчайшие сроки. Разработанная методика FOSY (FOcused SpectroscopY) позволяет преодолеть данные ограничения, проводя отнесение сигналов интересующего участка в течение нескольких часов без последующего трудозатратного анализа полученных спектров. Апробация данного подхода была успешно проведена на Тау-белке (441 а.о.), для которого ранее не удавалось получить полного и достоверного отнесения сигналов, необходимого для обнаружения его функционально-активных сайтов посттрансляционных модификаций. Применения методики FOSY позволило достоверно определить два ключевых сайта фосфорилирования. А как известно, избыточное фосфорилирование Тау-белка при болезни Альцгеймера и Паркинсона приводит к образованию нейрофибриллярных клубков и патологиям стабилизации аксональных микротрубочек.
- 2021 Unambiguous tracking of protein phosphorylation by fast high-resolution FOSY NMR. Angew Chem Int Ed Engl 60 (44) 23540–23544
Лаборатория моделирования биомолекулярных систем (Ефремов Р.Г.)
Структурный механизм тепловой активации ионного канала TRPV3
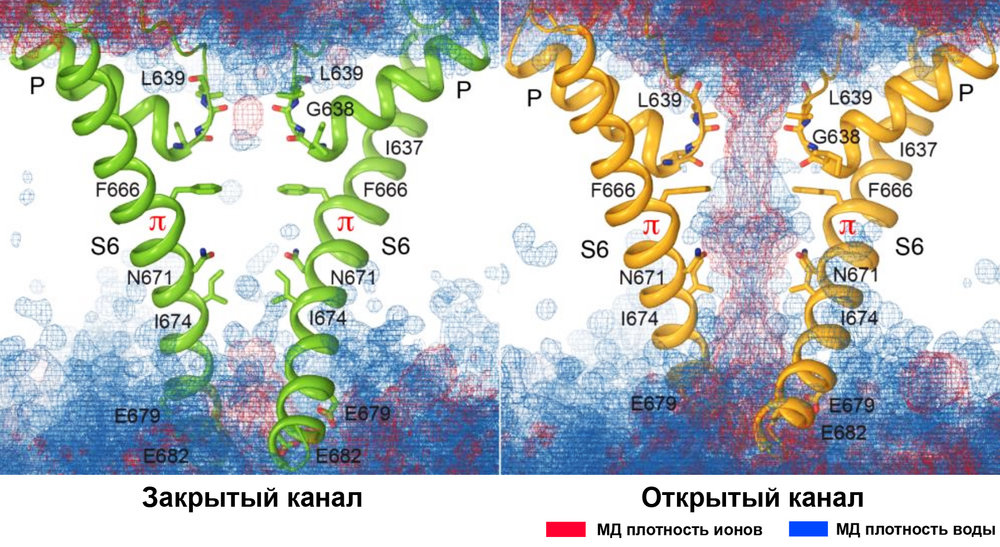
Ионный канал TRPV3 — один из представителей ванилоидного подсемейства термочувствительных каналов TRP (термо-TRP), экспрессирующийся преимущественно в клетках кожи (кератиноцитах). TRPV3 участвует в работе систем организма ответственных за кожную чувствительность, включая чувствительность к повышенным температурам (>31-39° C) и зуду, ноцицепцию (болевую чувствительность), поддержание кожного барьера, заживление ран, рост волос, эмбриональное развитие. Коллегами из Колумбийского университета (США) методом криоэлектронной микроскопии получены атомарные структуры белка в трех состояниях: закрытом, сенситизированном (переходном) и, впервые, - открытом при помощи температуры. На основании структурных данных был предложен механизм термоактивации канала, который сопровождается т.н. «конформационной волной» перестроек полипептидной цепи белка и его липидного окружения. Моделирование молекулярной динамики (МД) позволило охарактеризовать проводимость ионов и молекул воды через пору TRPV3 в различных состояниях и проследить за динамикой ключевого липида в т.н. «ванилоидном кармане». Эти липиды, по-видимому, играют роль своеобразных «плавких предохранителей», регулирующих перестройки белка в ответ на изменение температуры.
- 2021 Structural mechanism of heat-induced opening of a temperature-sensitive TRP channel. Nat Struct Mol Biol 28 (7) 564–572
Лаборатория молекулярной токсинологии (Уткин Ю.Н.)
,Лаборатория клеточных взаимодействий (Сапожников А.М.)
,Отдел молекулярной нейроиммунной сигнализации (Цетлин В.И.)
,Лаборатория лиганд-рецепторных взаимодействий (Кашеверов И.Е.)
Фосфолипазы А2 из ядов змей защищают клетки от вируса SARS-CoV-2
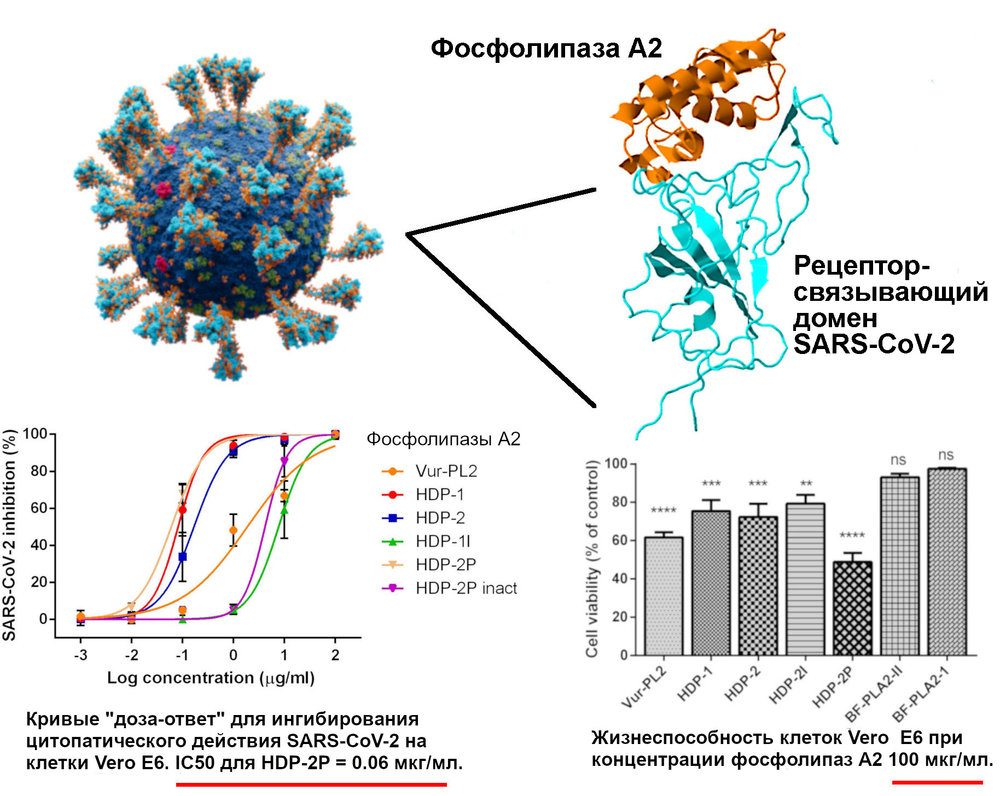
Фосфолипазы А2 (ФЛА2) из змеиного яда защищают клетки Vero E6 от цитопатического эффекта SARS-CoV-2. ФЛА2 показали низкую цитотоксичность по отношению к клеткам Vero E6, которая проявлялась при микромолярных концентрациях, но сильную противовирусную активность, обнаруживаемую при наномолярных концентрациях. ФЛА2 гадюки Никольского (Vipera nikolskii) проявила особенно сильный вирулицидный и противовирусный эффекты, связанные с фосфолиполитической активностью, и ингибировала слияние клеток, опосредованное взаимодействием гликопротеина S SARS-CoV-2 c ангиотензин-превращающим ферментом (АСЕ2). Более того, ФЛА2 препятствуют связыванию анти-АСЕ2 антител с ACE2 на поверхности клеток, а также рецептор-связывающего домена гликопротеина S с ACE2, что было показано методами проточной цитометрии и поверхностного плазмонного резонанса. Таким образом ФЛА2 могут предотвращать проникновение вируса в клетку, ингибируя его связывание с ACE2.
- 2021 Snake venom phospholipase A2s exhibit strong virucidal activity against SARS-CoV-2 and inhibit the viral spike glycoprotein interaction with ACE2. Cell Mol Life Sci 78 (23) 7777–7794
Лаборатория внесинаптической передачи (Семьянов А.В.)
Дистрофия астроцитов в стареющем мозге сопровождается нарушением синаптической пластичности

Возрастные изменения в структуре и функциях астроцитов и их влияние на снижение когнитивных функций в стареющем мозге на сегодняшний день недостаточно изучены. Используя двухфотонную микроскопию в сочетании с трехмерной реконструкцией, анализом по Шоллю и анализом объемной фракции неразрешённых астроцитарных отростков, мы показали значительное снижение площади территориальных доменов астроцитов, сокращение количества и длины оптически разрешённых астроцитарных отростков, снижение объёмной доли терминальных (оптически не разрешённых) отростков, снижение числа межастроцитарных клеточных контактов в стареющем мозге мышей С57Bl6. Исследование физиологии астроцитов с помощью фиксации астроцитарных токов методом патч-кламп и визуализации кальциевых сигналов выявили снижение калиевого тока и удаления глутамата, а также пространственно-временную реорганизацию кальциевых событий в астроцитах стареющих животных. Эти изменения происходили на фоне нарушения синаптической долговременной потенциации (LTP) в CA1 гиппокампа у стареющих мышей. Наши результаты могут объяснить астроглиальные механизмы возрастного снижения обучаемости и памяти.
- 2021 Astrocyte dystrophy in ageing brain parallels impaired synaptic plasticity. Aging Cell 20 (3) e13334
Отдел геномики адаптивного иммунитета (Чудаков Д.М.)
Предикция ответа на анти-PD-L1 иммунотерапию при раке мочевого пузыря
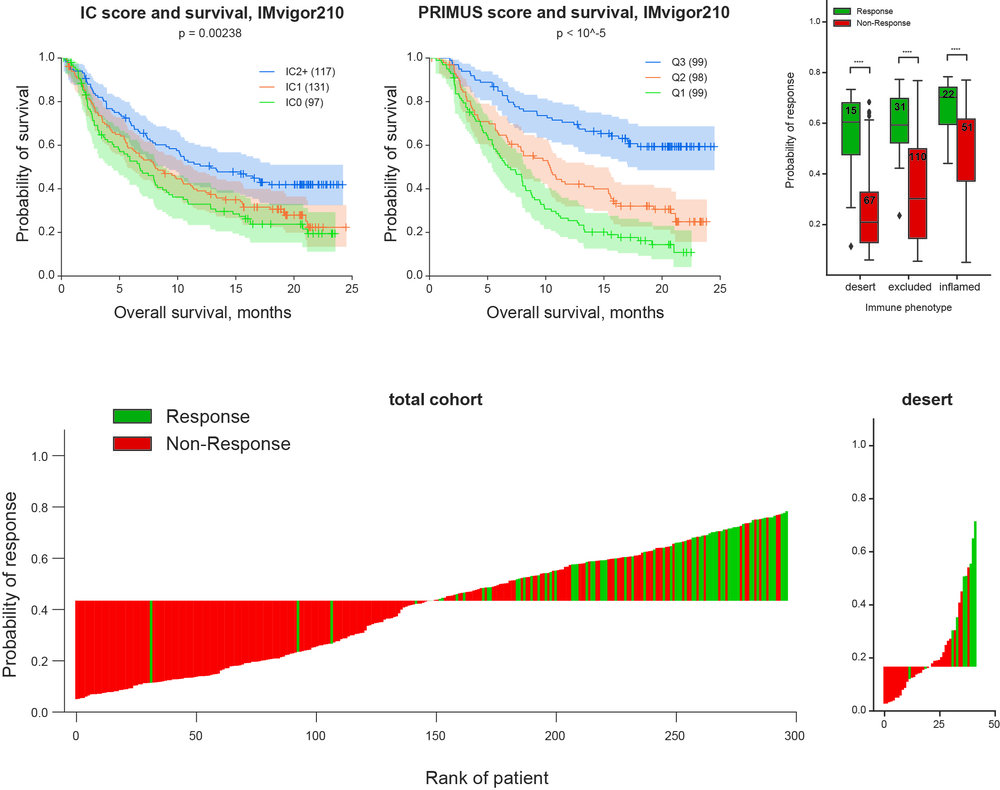
Показано, что нормировка цитотоксической сигнатуры на степень инфильтрации опухоли иммунными клетками драматически увеличивает точность предикции ответа на анти-PD-L1 иммунотерапию.
Показано, что соотношение IgG1/IgA экспрессии в опухолевым окружении является важным и независимым прогностическим и предиктивным маркером ответа на анти-PD-L1 иммунотерапию.
Разработан предиктор ответа анти-PD-L1 иммунотерапию, позволяющий надежно идентифицировать респондеров среди пациентов с инвазивной уротелиальной карциномой, включая подгруппу с низкоинфильтрированным “desert” фенотипом опухоли.
- 2022 Accounting for B-cell behavior and sampling bias predicts anti-PD-L1 response in bladder cancer. Cancer Immunol Res 10 (3) 343–353
Лаборатория сравнительной и функциональной геномики (Лебедев Ю.Б.)
,Лаборатория методов иммуносеквенирования (Чудаков Д.М.)
Динамика формирования Т-клеток памяти при легкой форме COVID-19
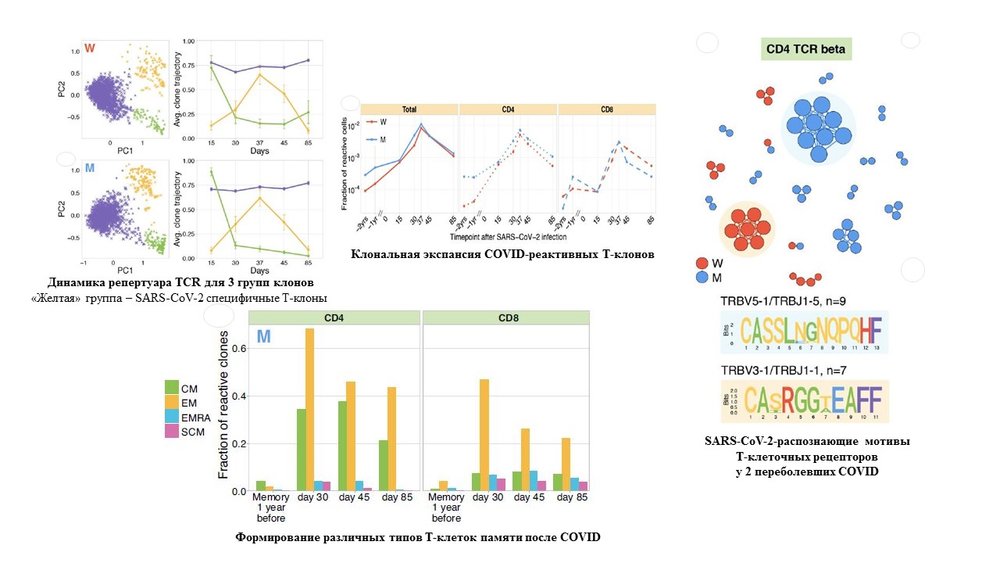
Мы применили масированное секвенирование Т-клеточных рецепторов (TCR) для отслеживания изменений в репертуаре Т-клеток после двух легких случаев COVID-19. У обоих доноров мы идентифицировали клоны CD4 + и CD8 + Т-клеток с высокой клональной экспансией после заражения. Антигенная специфичность CD8 + TCR к эпитопам SARS-CoV-2 была подтверждена как связыванием с тетрамером рMHC, так и структур найденных нами TCR с TCR, присутствующих в международных базах данных SARS-CoV2-специфичных TCR. Мы описываем характерные мотивы в CDR3-последовательностях TCR T-клонов, реагирующих на COVID-19. Мы показываем, что у обоих доноров большинство инфекционно-реактивных клонотипов приобретают фенотипы памяти. Определенные клоны Т-клеток были обнаружены во фракции памяти в момент времени до заражения, что свидетельствует об участии ранее существовавших перекрестно-реактивных Т-клеток памяти в иммунном ответе на SARS-CoV-2.
- 2021 Longitudinal high-throughput TCR repertoire profiling reveals the dynamics of T-cell memory formation after mild COVID-19 infection. Elife 10 1–17
Группа метаболических основ патологии (Билан Д.С.)
,Лаборатория молекулярных технологий (Белоусов В.В.)
Динамика развития ацидоза и окислительного стресса в нейронах в острой фазе ишемического инсульта
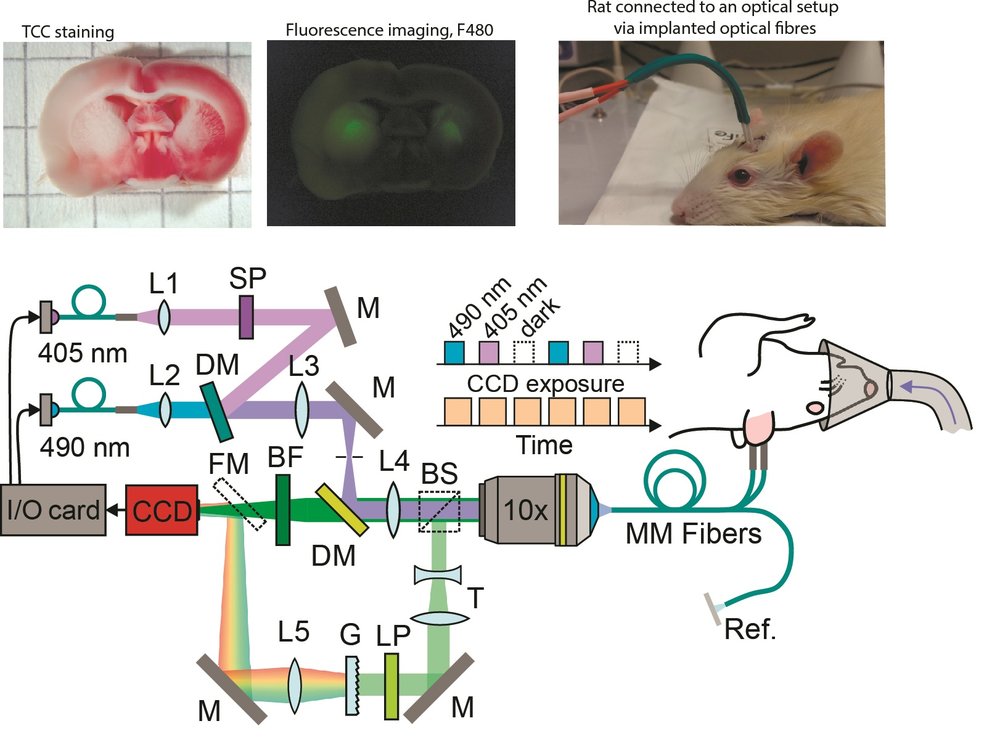
Ишемический инсульт является одной из главных причин смертности и инвалидизации населения в мире. Патофизиология инсульта активно исследуется на самых разных уровнях и моделях, однако до сих пор существуют серьезные пробелы в понимании метаболических изменений, сопровождающих данное заболевание. Особенно плохо изучены процессы, которые происходят в ткани мозга на самых ранних стадиях ишемии и реперфузии. В сотрудничестве с коллегами из Федерального центра мозга и нейротехнологий ФМБА России, Московского Государственного Университета имени М.В. Ломоносова и других российских и зарубежных институтов мы разработали технологию, позволяющую регистрировать биохимические события в тканях мозга лабораторных животных in vivo.
Путем вирусной доставки в мозге крыс линии SHR были экспрессированы разработанные ранее в нашем институте генетически кодируемые флуоресцентные биосенсоры SypHer3s для регистрации динамики рН (Ermakova et al. Chem. Commun. 2018 doi:10.1039/C7CC08740C) и HyPer7 для регистрации пероксида водорода (H2O2) (Pak et al., Cell Metabolism 2020 doi:10.1016/j.cmet.2020.02.003). Флуоресцентный рациометрический сигнал биосенсоров считывался с помощью специально разработанной системы двухканальной фотометрии через имплантированные в мозг оптические волокна. Ишемический инсульт вызывался путём перекрытия средней мозговой артерии животного (MCAO). Мы зарегистрировали мощный ацидоз в ишемизированной ткани мозга, возникающий с первых секунд развития патологии. Вопреки ожиданиям, значительного образования H2O2, одного из главных представителей активных форм кислорода в клетках, в острой фазе ишемии/реперфузии обнаружено не было. Существенное увеличение концентрации H2O2 в митохондриях нейронов в поврежденной ткани наблюдалось лишь на следующие сутки.
Сравнение результатов экспериментов in vivo с исследованиями на культивируемых нейронах в условиях гипоксии/реоксигенации продемонстрировало, что динамика окислительно-восстановительных процессов в этих моделях значительно различается. Это в очередной раз подтверждает, что культура клеток является плохой прогностической моделью метаболических событий, происходящих внутри организма.
- 2021 In vivo dynamics of acidosis and oxidative stress in the acute phase of an ischemic stroke in a rodent model. Redox Biol 48 102178
2020 год
Исследования и разработки 2020 года, готовые к практическому применению
Тест-системы к COVID-19 и моноклональные антитела HFB30132A
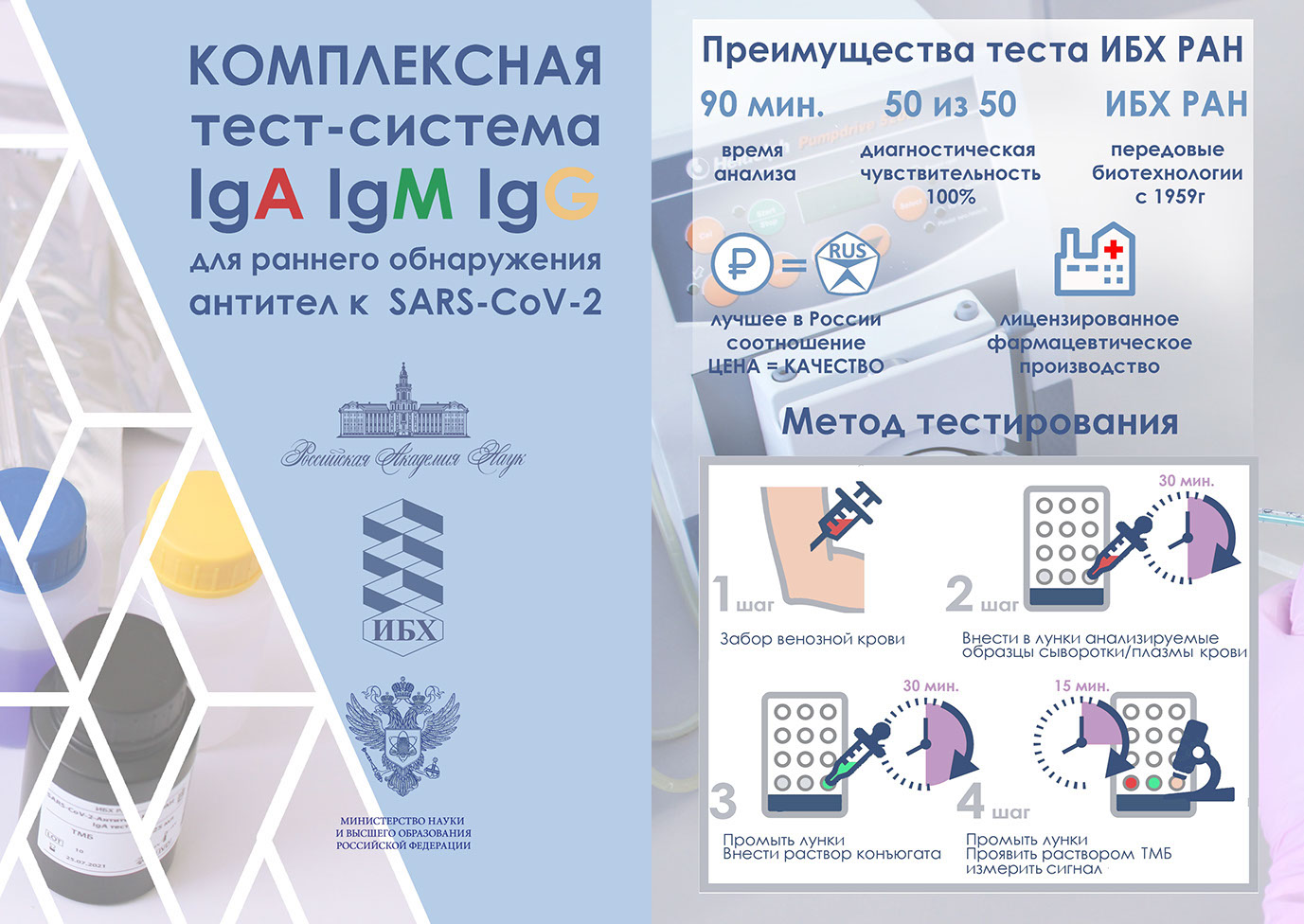
Во-первых, учеными ИБХ РАН, в сотрудничестве с ЦКБ РАН при участии Российской академии наук и Министерства науки и высшего образования РФ, разработаны тест-системы к COVID-19. Тест-системы прошли сертификацию Росздравнадзора РФ и в настоящее время запущены в производство. Тест-системы представлены в четырёх вариантах: общий скрининговый тест (суммарное определение сразу трех антител IgA, IgG, IgM) и три системы для определения конкретного класса антител (IgA-, IgG- или IgM-антител).
Во-вторых, ИБХ РАН, ПАО «Фармсинтез» и международная биофармацевтическая компания HiFiBio Therapeutics подписали соглашения, в рамках которых участники объединят свои компетенции для проведения клинических испытаний, производства и поставок на российский рынок моноклонального антитела HFB30132A для лечения и профилактики коронавирусной инфекции SARS-CoV-2. Ранее проект был одобрен руководством Министерства здравоохранения и Минпромторга РФ.
В сочетании с разработкой рекомбинантной композитной генно-инженерной вакцины против вакцины SARS-CoV-2 организация производства нейтрализующего антитела против вируса SARS-CoV-2 формирует уникальный портфель с полным иммунобиологическим покрытием инфекции SARS-CoV-2: профилактическая вакцинация, экстренная иммунопрофилактика, иммунотерапия. Результаты проведенных в мире научных исследований сегодня позволяют говорить о том, что первое поколение вакцин, создаваемых для профилактики SARS-CoV-2 инфекции, вероятно не сможет в полной мере взять под контроль распространение вируса SARS-CoV-2. В этих условиях расширение арсенала средств специфической иммунотерапии SARS-CoV-2 инфекции приобретает критическое значение.
Лаборатория биокатализа (Габибов А.Г.)
,Лаборатория химии протеолитических ферментов (Смирнов И.В.)
С помощью квантово-механического молекулярно-механического (QM/MM) подхода объяснено изменение стереопецифичности антител
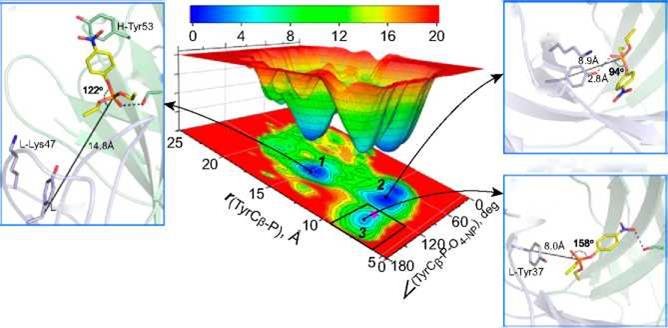
Разработан новый подход на основе метода квантовой механики/молекулярной механики (QM/MM) и funnel-метадинамики с использованием возможностей суперкомпьютера для направленного изменения реакционной способности иммуноглобулинов (Ig). Это было достигнуто за счет определения позиций и типа аминокислотных остатков для замены в каталитическом центре, что позволило обеспечить усиление нуклеофильности атакующего остатка Тирозина 37. Оптимизированный с точки зрения вычислений вариант, L-Leu47Lys, обеспечивает 340-кратное увеличение реакционноспособной полученного мутантного варианта по сравнению с Ig-параоксоназой дикого типа в результате индуцированной субстратом ионизации остатка Тирозина 37. Этот универсальный алгоритм был с успехом использован для объяснения стереоселективности мутантных антител по отношению к Р-хиральному фенилфосфонату. Эти расчеты были подтверждены кинетическими и кристаллографическими методами.
- 2020 Multiscale computation delivers organophosphorus reactivity and stereoselectivity to immunoglobulin scavengers. Proc Natl Acad Sci U S A 117 (37) 22841–22848
Лаборатория биокатализа (Габибов А.Г.)
Открыт фермент – киназа AmiN, обеспечивающую резистентность к антибиотику амикумацину.
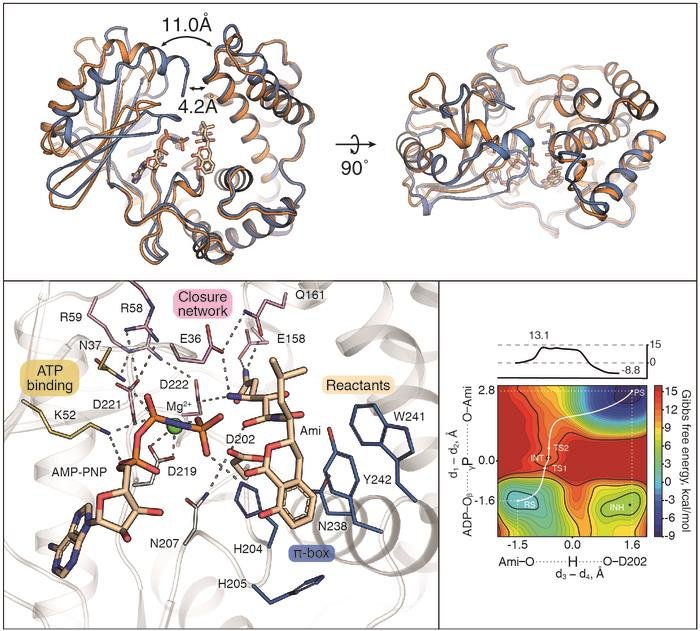
Открыт фермент – киназа AmiN, обеспечивающую резистентность к антибиотику амикумацину. Уникальность данной киназы заключается в ее необычайно высоком сродстве к субстрату, позволяющему высокоэффективно элиминировать даже следовые количества антибиотика в диапазоне наномолярных концентраций. Комплекс методов, включающих рентгеноструктурный анализ и математическое моделирование, позволил детально исследовать совершенный механизм катализа, связанный с закрытием активного центра фермента.
- 2020 A kinase bioscavenger provides antibiotic resistance by extremely tight substrate binding. Sci Adv 6 (26) eaaz9861
Лаборатория биокатализа (Габибов А.Г.)
,Лаборатория белков гормональной регуляции (Белогуров А.А.)
,Лаборатория химии протеолитических ферментов (Смирнов И.В.)
,Лаборатория биоинформационных методов комбинаторной химии и биологии (Андреев Д.Е.)
Разработана математическая модель, являющаяся основой для рационализации амплификации библиотек с использованием ePCR.
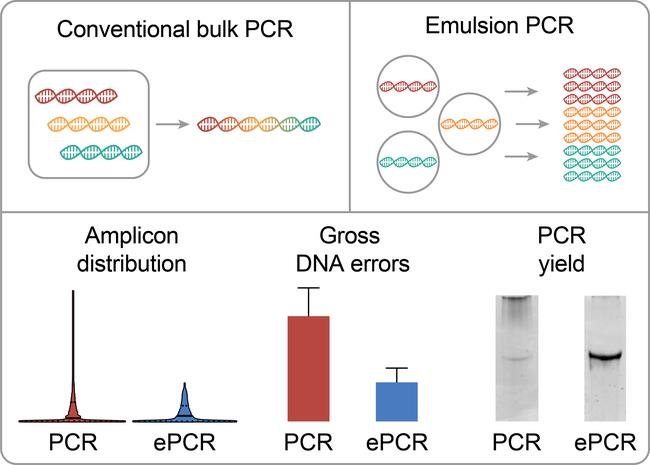
Показано, что амплификация отдельных молекул ДНК, инкапсулированных в огромном количестве капель эмульсии (ePCR), позволяет решить эту проблему. Различные режимы ePCR были экспериментально проанализированы, чтобы определить наиболее совершенные методы амплификации библиотек ДНК. На основе полученных экспериментальных данных была разработана математическая модель, являющаяся основой для рационализации амплификации библиотек с использованием ePCR. Детальное описание ампликонов библиотек ДНК было получено в результате высокопроизводительного секвенирования, подчеркивающего основные преимущества ePCR по сравнению с обычной PCR. ePCR снижает частоту возникновения грубых ошибок в процессе ДНК амплификации и обеспечивает более равномерное распределение амплифицированных последовательностей. Таким образом, благодаря ePCR достигается квазимономолекулярная амплификация, представляющая собой фундаментальное требование при амплификации сложных матриц. Исследователи показали, что ePCR препятствует дегенерации разнообразия и обеспечивает сохранение качества библиотек ДНК.
- 2020 Liquid drop of DNA libraries reveals total genome information. Proc Natl Acad Sci U S A 117 (44) 27300–27306
Лаборатория молекулярной иммунологии (Деев С.М.)
,НПП «Питомник лабораторных животных» (Телегин Г.Б.)
Стратегия синергичной комбинированной адресной иммуно/химиотерапии агрессивных опухолей с визуальным контролем.
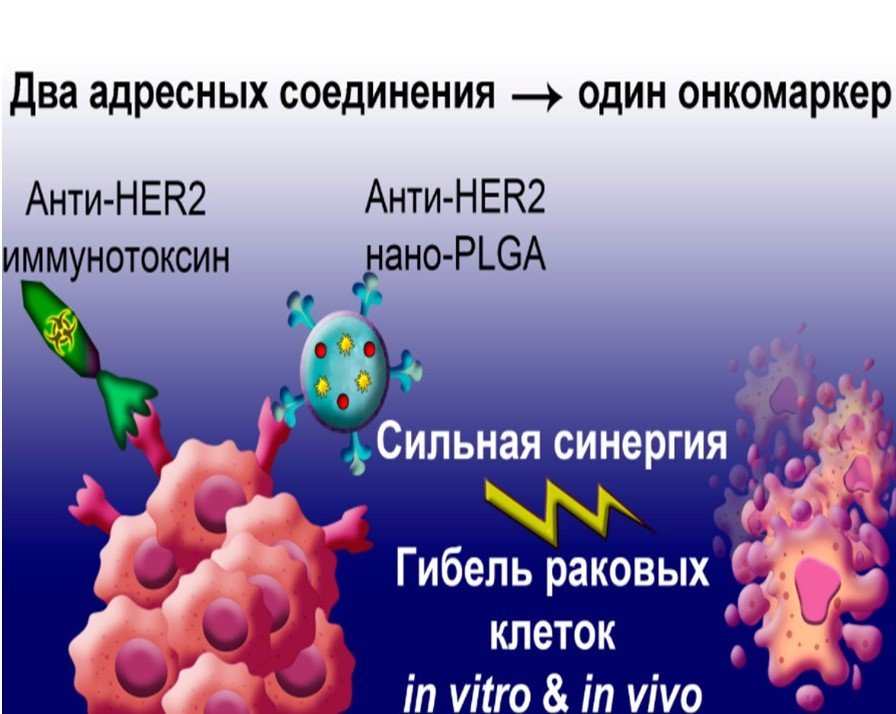
Впервые для улучшенной терапии опухолей с визуальным контролем разработана стратегия региоспецифичного нацеливания на разные участки одного и того же рецептора опухолевой клетки комбинации двух противоопухолевых токсинов с разными механизмами действия - антибиотика доксорубицина в составе адресных наночастиц с диагностическим флуоресцентным красителем и белкового адресного токсина. Показано строгое синергетическое действие этих токсинов на опухоль, которое позволило снизить действующую дозу противоопухолевых токсинов в 1000 раз в опытах in vitro и существенно улучшить терапевтический эффект in vivo. Данная стратегия позволила замедлить рост опухоли и предотвратить появления метастазов.
- 2020 Dual Regioselective Targeting the Same Receptor in Nanoparticle-Mediated Combination Immuno/Chemotherapy for Enhanced Image-Guided Cancer Treatment. ACS Nano 14 (10) 12781–12795
Отдел биомолекулярной химии (Ямпольский И.В.)
,Лаборатория молекулярной иммунологии (Деев С.М.)
,Лаборатория экспрессионных систем и модификации генома растений (Долгов С.В.)
,Лаборатория химии метаболических путей (Ямпольский И.В.)
,Группа синтетической биологии
,Группа метаболической инженерии растений
,Группа молекулярных меток для оптической наноскопии (Мишин А.С.)
Создание растений с генетически кодируемой биолюминесценцией
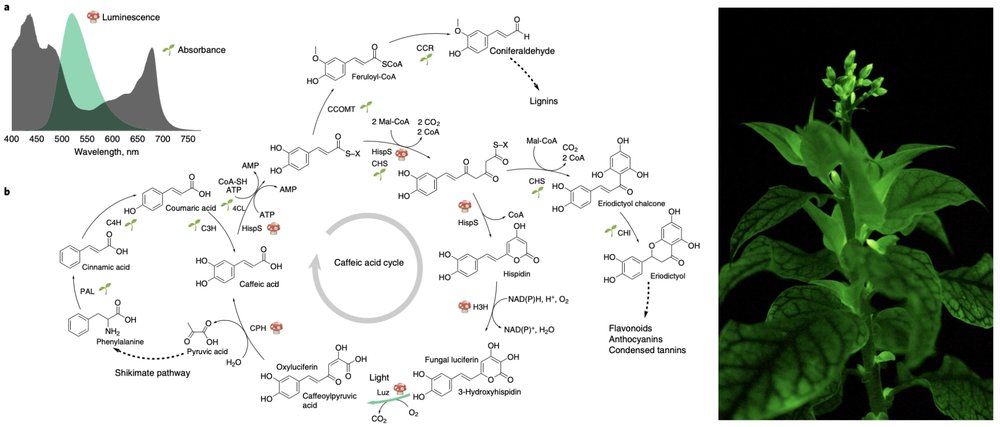
В статье, опубликованной в журнале Nature Biotechnology, ученые ИБХ РАН показали возможность создания растений, излучающих собственную видимую люминесценцию. Было обнаружено, что биолюминесценция некоторых грибов метаболически сходна с естественными процессами, характерными для растений. Интегрировав гены биолюминесцентной системы гриба Neonothopanus nambi в геном табака, ученые смогли создать растения, которые светятся намного ярче, чем это было возможно ранее. Созданные трансгенные растения светятся непрерывно на протяжении всего жизненного цикла и могут быть использованы в качестве системы для проведения биоимиджинга. В отличие от других широко используемых биолюминесцентных систем, например, светлячков, для поддержания биолюминесценции грибов не требуются уникальные химические реагенты.
- 2020 Plants with genetically encoded autoluminescence. Nat Biotechnol 38 (8) 944–946

