Пресс-центр / новости / СМУ /
Видео и статья по 28-му семинару СМУ «Синтез люциферина люминесцентного червя Fridericia heliota и его аналогов»
19 октября 2015 года в ИБХ РАН состоялся 28-й семинар СМУ, посвященный биолюминесценции и роли химического синтеза в установлении структуры биологических молекул. Участники семинара с интересом прослушали доклад научного сотрудника Группы синтеза природных соединений Александры Царьковой «Синтез люциферина люминесцентного червя Fridericia heliota и его аналогов». После доклада состоялась научная дискуссия, посвященная проблемам расшифровки химического механизма данного явления. Участники дискуссии высказали предположения о том, зачем вообще малощетинковым червям нужна биолюминесценция.
Биолюминесценция — это явление излучения света живыми организмами. Основную роль в этом процессе играют фермент — люцифераза — и субстрат, называемый люциферином, при окислении которого происходит образование оксилюциферина в возбужденном состоянии с последующим испусканием видимого света. Это явление достаточно распространено в живой природе – на сегодняшний день известно около 700 родов живых существ, принадлежащих к 17 типам в составе 4 царств, представители которых обладают способностью к биолюминесценции. Известно, что существует около 30 различных химических механизмов, благодаря действию которых живые существа могут испускать свет. И, тем не менее, ученые до сих пор открывают все новые и новые разновидности биолюминесцентных систем.
Одна из них – уникальная биолюминесцентная система малощетинкового червя Fridericia heliota – была описана сотрудниками группы Синтеза природных соединений Института биоорганической химии имени академиков М. М. Шемякина и Ю. А. Овчинникова Российской академии наук (ИБХ РАН) совместно с сотрудниками лаборатории Биомолекулярной ЯМР-спектроскопии. О том, как ученым удалось это сделать, рассказала одна из участников данного исследования, аспирантка Александра Царькова на 28-м семинаре СМУ ИБХ: «Синтез люциферина люминесцентного червя Fridericia heliota и его аналогов».

научный сотрудник группы Синтеза природных соединений Александра Царькова
«Несмотря на то, что по современным оценкам, существует около 30 различных химических механизмов биолюминесценции», – рассказывает Александра Царькова – «до недавнего времени было известно лишь семь люциферинов, причем структура последнего из них была расшифрована около 25 лет тому назад – это было светящееся вещество панцирных жгутиконосцев Dinoflagellata.
Если говорить вообще о светящихся представителях класса Oligochaeta, то долгое время существовала концепция о единой природе люминесценции этих существ. Она опиралась на результаты сравнительного исследования биохимии двенадцати видов малощетинковых червей. Все они секретировали биолюминесцентную слизь. Интересно, что биолюминиесценция всех исследованных олигохет характеризовалась одним общим признаком – в ней активно участвует перекись водорода. Также необходимо отметить, что единственные люцифераза и люциферин малощетинковых червей, чья структура на данный момент установлена – это фермент и субстрат червя Diplocardia longa – вступают в перекрёстные реакции с другими одиннадцатью люциферинами и люциферазами олигохет.
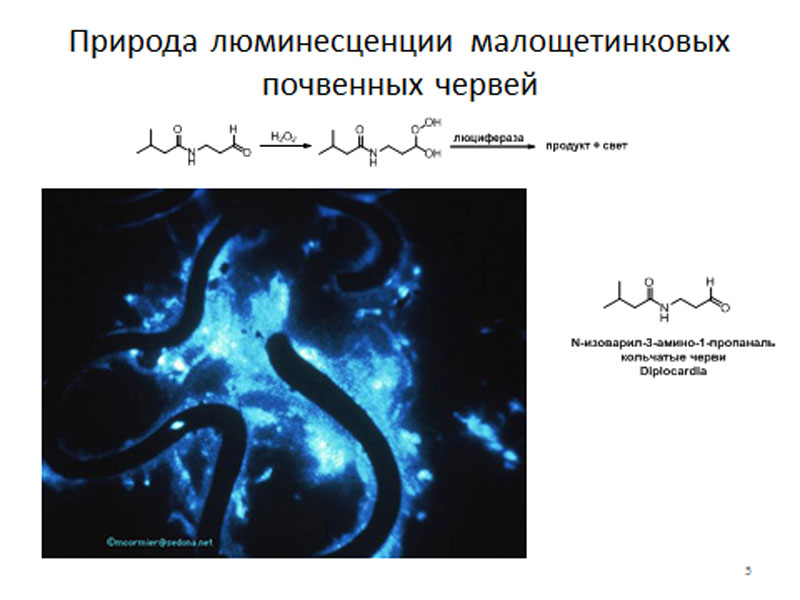
типичная биолюминесценция олигохет
Что касается феномена биолюминесценции почвенных малощетинковых червей из семейства Enchytraeidae, ограничивающийся родами Henlea и Fridericia, то до недавнего времени он оставался практически неизученным. Все началось с того, что совсем недавно нашими коллегами из Красноярска, Валентином Петушковым и Натальей Родионовой был открыт новый вид из рода Fridericia – это та самая Fridericia heliota. Это небольшие бело-желтые черви, которые начинают светиться голубым светом в ответ на механическую стимуляцию. Следует заметить, что биолюминесценция Fridericia heliota отличается от таковой всех ранее изученных олигохет – она локализована в эпидермальных клетках, и никакой светящейся слизи при этом не выделяется. Если после механической стимуляции посмотреть на этого червя в темноте, то становятся заметны светлые точки по всему телу, которое само остается темным.
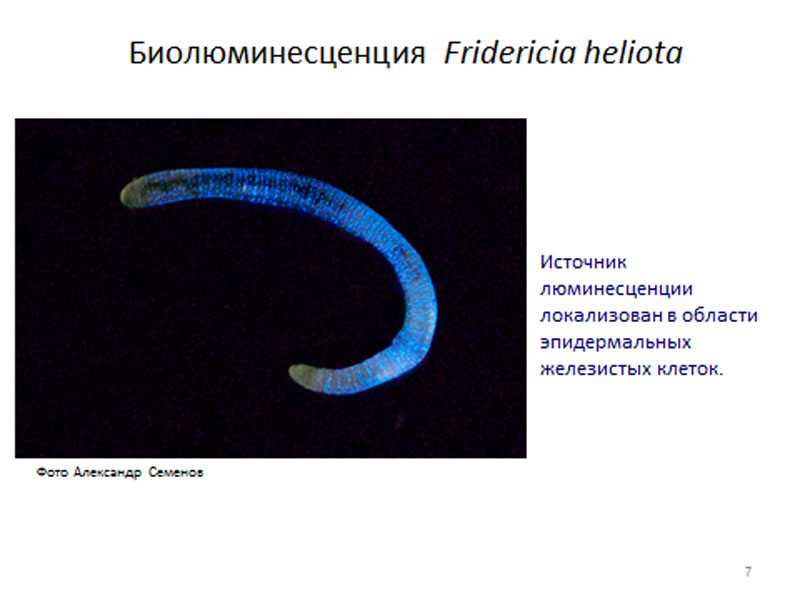
биолюминесценция Fridericia heliota
Люминесцентная система Fridericia heliota насчитывает пять компонентов –это сам люциферин, люцифераза, АТФ, ионы магния и кислород. Следует заметить, что выделение и определение всех компонентов этой системы было сильно затруднено из-за того, что данных червей было сложно искать, а также из-за малого количеством люциферина в биомассе найденных экземпляров. Червей приходилось разыскивать зимой в сибирской тайге по ночам – если учесть, что размеры данной олигохеты составляют 10-15 мм в длину, то можно представить, насколько сложной была эта задача. Поиск происходил следующим образом – землю собирали в мешки, потом ее просеивали, далее сортировали найденные виды (поскольку в этих е местах обитают и представители рода Henlea). Каждый сбор давал примерно 30 г необработанной биомассы червя. Содержание же люциферина составляло примерно 0,1 мкг на грамм биомассы. Таким образом, после обработки 150 г биомассы червя было получено всего 5 мкг люциферина. С таким маленьким количество вещества было весьма непросто работать.
Однако к счастью для нас, в процессе выделения люцифериновой фракции мы наткнулись на содержащиеся в ней вещества неопределённого состава, которые обладали хроматографической подвижностью, а также имели спектральные свойства, очень похожие на люциферин. Мы предположили, что эти вещества могут являться либо аналогами, либо предшественниками люциферина – или же продуктами его деградации. Следует заметить, что по количеству эти соединения в 20-30 раз превосходили таковое люциферина. Мы назвали эти вещества CompX и AsLn2.
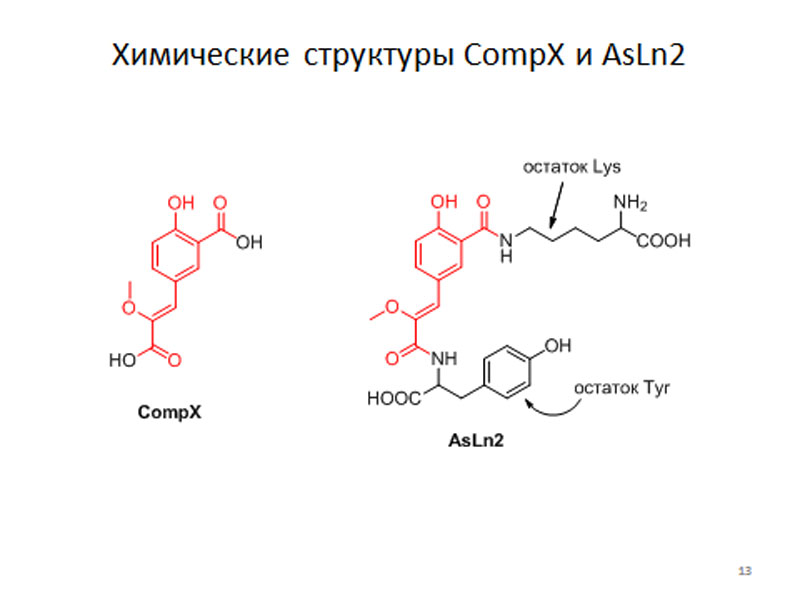
CompX и AsLn2
После этого мы решили опередить структуру CompX и затем синтезировать это вещество. Согласно данным ЯМР, которые предоставил нам Максим Дубинный, это вещество оказалось модифицированным тирозином. Он получается в результате трех модификаций: дезаминирования, метилирования енола, а затем карбоксилирования в ароматическое кольцо. ЯМР спектральные данные были недостаточны для определения конфигурации двойной связи этого соединения, в связи с чем был предпринят синтез обоих изомеров – для того, чтобы потом сравнить ЯМР-данные синтетического и природного веществ. Ключевой стадией синтеза CompX являлась реакция олефинирования, которая позволила нам получить оба изомера в соотношении 2:1 (Z к E). Мажорный изомер Z-CompX был абсолютно идентичен природному соединению по своим спектральным данным. А вот другой изомер резко отличался от природного аналога, и, кроме того, он не обладал флуоресцентными свойствами.
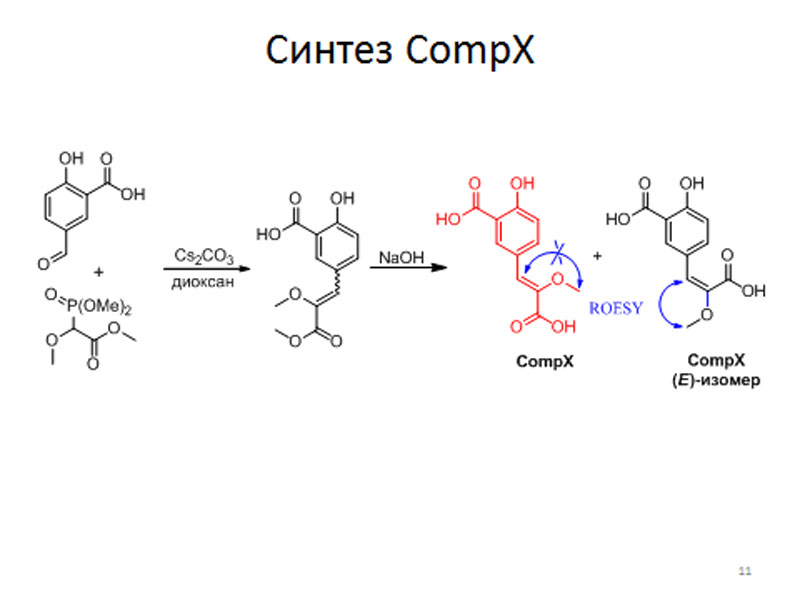
синтез CompX
Дальнейшие ЯМР-исследования обнаружили наличие характерного для природного CompX паттерна ароматических протонов в спектрах самого люциферина, а также его аналогов. Таким образом, нам удалось установить, что это вещество является структурным фрагментом люциферина.
Далее, на основании данных дальнейших ЯМР- и масс-спектрометрических исследований мы выяснили структуру другого обнаруженного нами вещества, AsLn2. Выяснилось, что это модифицированный трипептид, в котором карбоксильные группы CompX вовлечены в образование пептидных связей с остатками лизина и тирозина. Это предположение так же было подтверждено методом встречного синтеза, в котором метиловый эфир CompX был последовательно введен в конденсации с L-лизином и L-тирозином. В результате пятистадийного синтеза этого был получен AsLn2 с выходом в 14 процентов. Спектральные данные ЯМР продукта последней стадии синтеза оказались идентичны природному образцу, что позволило предположить идентичность порядка химических связей в соединении AsLn2.
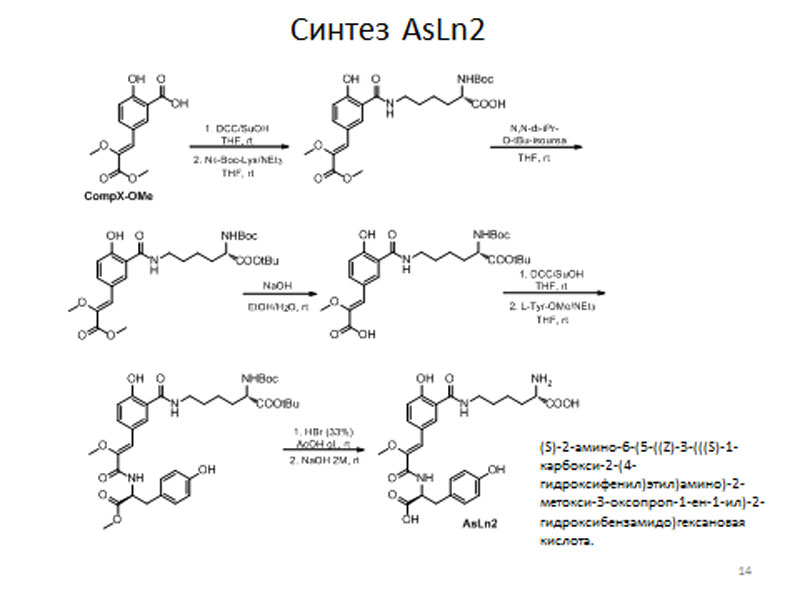
синтез AsLn2
К сожалению, в нашем распоряжении было немного природного аналога AsLn2, поэтому мы не смогли определить его стереохимическую конфигурацию. Для того, чтобы сделать это, синтетический и природный AsLn2 были прогнаны через хиральную колонку и выяснилось, что времена удерживания обоих веществ были совершенно идентичными. Полученные данные позволили предположить L-конфигурацию обоих стереоцентров в молекуле. Таким образом была установлена стереохимическая структура полученного нами AsLn2.
Наконец мы начали работу по определению структуры самого люциферина. Однако из-за того, что его было очень мало, всего 5 мкг, нам удалось получить лишь частичные протонные спектры ЯМР. Однако из этих данных следовало, что в молекуле люциферина присутствуют три фрагмента – остаток CompX, L-лизин, и остаток гамма-аминомасляной кислоты (ГАМК), которые в сумме давали нам вещество следующего состава: С21Н29N3О8. Но эта формула противоречила данным масс-спектрометрии высокого разрешения, согласно которым вещество должно было иметь формулу С23Н29N3О11. Для того, чтобы понять, куда делись отсутствующие атомы, мы как бы вычли одну формулу из другой и получили фрагмент С2О3, который соответствует оксалату. Таким образом, мы выявили четвертый недостающий фрагмент люциферина.
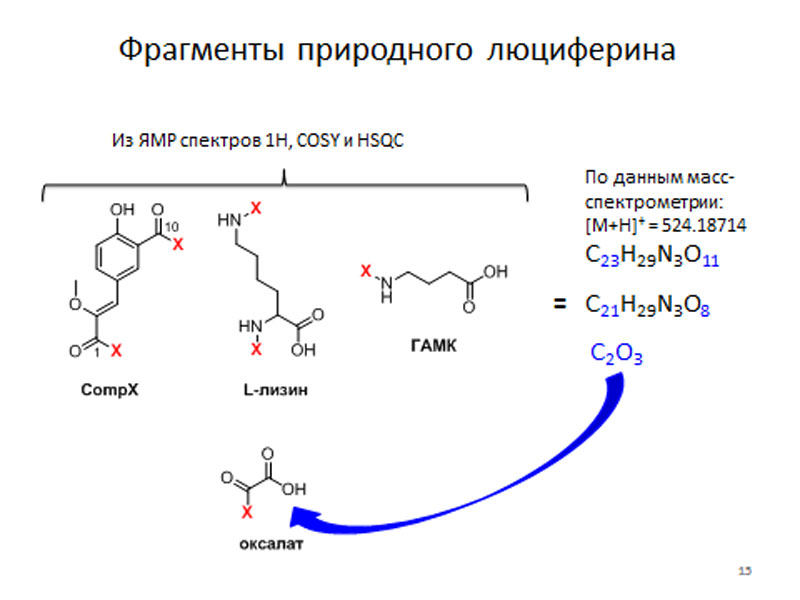
четыре фрагмента люциферина
Итак, нам стало ясно, что молекула люциферина состоит 4х фрагментов: CompX, L-лизина, ГАМК и оксалата. Однако из этих четырех фрагментов получались четыре структуры, соответствующие полученным данным ЯМР и масс-спектрометрии – они различались лишь порядком пептидных связей, которые связывают данные фрагменты. Мы решили синтезировать все четыре варианта и сравнить их ЯМР-спектры со спектрами природного люциферина.
Основываясь на структуре аналога люциферина AsLn2, мы предположили, что в самом люциферине, также имеющим фрагмент лизина, эта аминокислота присоединена к С10- карбоксильной группе фрагмента CompX, в то время как ГАМК, вероятнее всего, присоединена к С1-карбоксильной группе. Это был первый изомер, который мы синтезировали. После этого его ЯМР-спектры были сравнены со спектрами природного люциферина, однако химические сдвиги протонов синтетического изомера оказались весьма близкими, но не идентичными таковым природного вещества. Более того, при смешивании с люциферазой Fridericia heliota (в присутствии АТФ и ионов магния) это вещество не светилось. Далее нами были синтезированы другие изомеры, с которыми поступили аналогичным образом. И только у одного из этих синтетических веществ ЯМР-спектр полностью совпал с таковым природного люциферина.
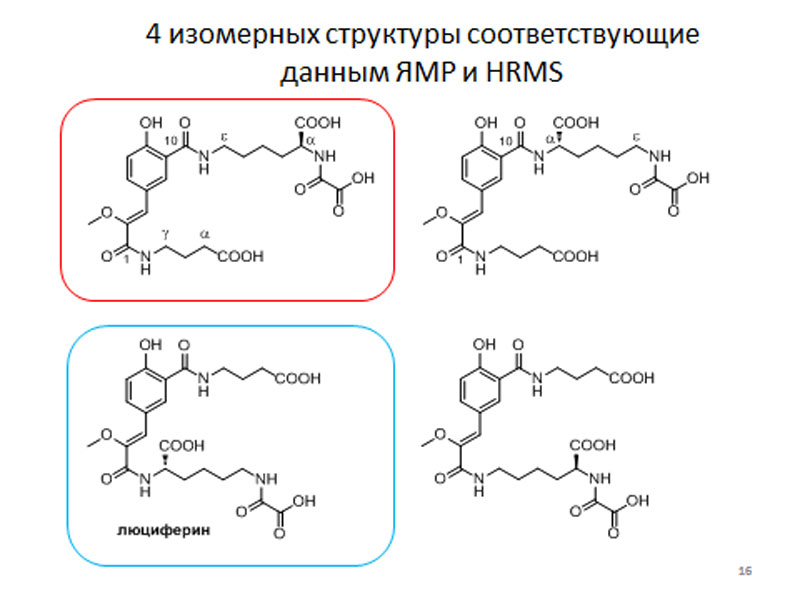
четыре изомера синтетического люциферина: красной рамкой выделен тот, что получился первым, а синей – тот, что оказался аналогичен природному веществу
Интересно также и то, что только этот изомер вступал в биолюминесцентную реакцию с люциферазой червя. Кроме того, зависимость интенсивности свечения синтетического люциферина от его концентрации была аналогичной той, что характерна для природного аналога.
Помимо аналогов CompX и AsLn2 из люцифериновой фракции червя Fridericia heliota был выделен еще один аналог – это дипептид AsLn7. По данным ЯМР-спектроскопии мы установили, что он состоит из CompX и остатка ГАМК. Но нам не было понятно, как два этих фрагмента соединяются друг с другом. Для того, чтобы понять это, мы прибегли к эксперименту ЯМР-титрования. Который провел Константин Минеев. Этот эксперимент позволил нам определить, что ГАМК присоединена к С10-карбоксильной группе CompX, в то время как С1-карбоксильная группа свободна. Этот же эксперимент позволил нам увидеть, что карбоксильная группа ГАМК также является свободной.
В связи с этим мы предположили, что AsLn7, скорее всего, является непосредственным предшественником люциферина червя Fridericia heliota. Это предположение основывалось на том, что он имеет два из четырех структурных фрагментов этого вещества, которые к тому же соединены в правильном порядке. Мы также подтвердили строение AsLn7 при помощи встречного синтеза, а затем сравнили данные ЯМР-спектров природного и синтетического аналогов. Эти спектры полностью совпали.
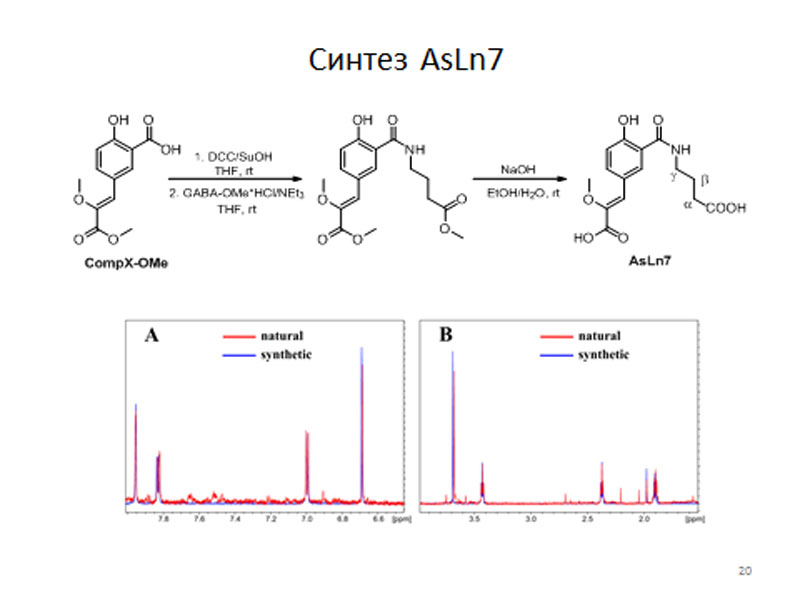
синтез AsLn7
Стоит сказать, что наличие в биомассе червя AsLn7, в структуру которого входят два из четырех фрагментов люциферина, позволяет предположить, что путь биосинтеза биолюминесцентного вещества Fridericia heliota лежит через последовательное соединение его четырех фрагментов. Все эти четыре компонента – CompX, лизин, ГАМК и оксалат – соединяются при помощи специфичных (или неспецифичных) аминокислотных лигаз, которые нам пока неизвестны. Сейчас мы работаем над тем, чтобы последовательно расшифровать непосредственные механизмы биосинтеза данного люциферина».
После доклада Александра Царькова, отвечая на вопросы присутствующих на семинаре, сформулировала еще одну задачу, которую следовало бы решить в ближайшее время. Дело в том, что структура люциферазы червя Fridericia heliota до сих пор остается неизвестной. По мнению докладчика, было бы неплохо исследовать строение данного фермента, а также найти ген, отвечающий за синтез люциферазы и расшифровать его структуру. Эти данные могли бы значительно ускорить процесс изучения механизма люминесценции червя Fridericia heliota.
Кроме того, в конце семинара состоялась интересная дискуссия по вопросу о том, зачем вообще этому маленькому червю, который постоянно живет в темноте, нужна биолюминесценция? Среди олигохет неизвестны случаи использования этого явления для привлечения партнера во время размножения – как это делают взрослые жуки-светляки (Lampyridae). Во время дискуссии Александра Царькова высказала предположение, что, возможно, биолюминесценция помогает этим крошечным созданиям отпугивать хищников, то есть поступать примерно так же, как каракатица Lycoteuthis diadema, использующая своих светящихся симбиотических бактерий именно в этих целях. По мнению Александры, в пользу этой версии говорит тот факт, что Fridericia heliota начинает светиться в ответ на механическую стимуляцию, то есть на обычное прикосновение. Таким образом, можно предположить следующую схему: хищник касается тела червя, тот в ответ начинает светиться и агрессор, испуганный вспышкой яркого света, поспешно удаляется.
Другую, не менее интересную версию, объясняющую данный феномен, предложил присутствовавший на семинаре ведущий научный сотрудник кафедры микробиологии МГУ им. М. В. Ломоносова доктор биологических наук Анвар Джураевич Исмаилов. Он заметил, что биолюминесценция часто свойственна организмам, которые обитают там, где наблюдается недостаток кислорода. В таких условиях в процессе окисления часто образуется перекись водорода, которая является источником активного кислорода и, тем самым, представляет опасность для живых существ. Испускаемый же живыми организмами свет способствует быстрому разложению этого опасного для них вещества. По мнению Анвара Джураевича, биолюминесценция может использоваться почвенными олигохетами именно в таких целях.

Александра Царькова отвечает на вопросы участников семинара
Обсудив эту версию, участники семинара согласились с тем, что такое вполне может быть. Однако, отметила Александра Царькова, все эти рассуждения пока что остаются чисто теоретическими, поскольку в настоящее время нет возможности экспериментально проверить какую-нибудь из предложенных версий. Дело в том, что ни одна из попыток создать популяцию червя Fridericia heliota в искусственной среде не увенчалась успехом – взятые из природы почвенные олигохеты не размножались в лабораторных условиях и быстро погибали. Это происходило даже тогда, когда для них воссоздавали условия, максимально близкие к таковым в их естественной среде обитания. Таким образом, не исключено, что загадку биолюминесценции червя Fridericia heliota можно будет разгадать только тогда, когда будет расшифрован весь механизм этого явления, а также определена структура люциферазы и кодирующего ее гена.
1 ноября 2015 года

