Пресс-центр / новости / Наука /
Проанализировали основные достижения ИБХ РАН за 2016 год
Первое в новом году заседание Ученого Совета ИБХ РАН открылось выступлением заместителя директора, академика Александра Габибовича Габибова. В ходе выступления были проанализированы работы всех подразделений Института за 2016 год.
Важнейшие достижения научных коллективов ИБХ РАН
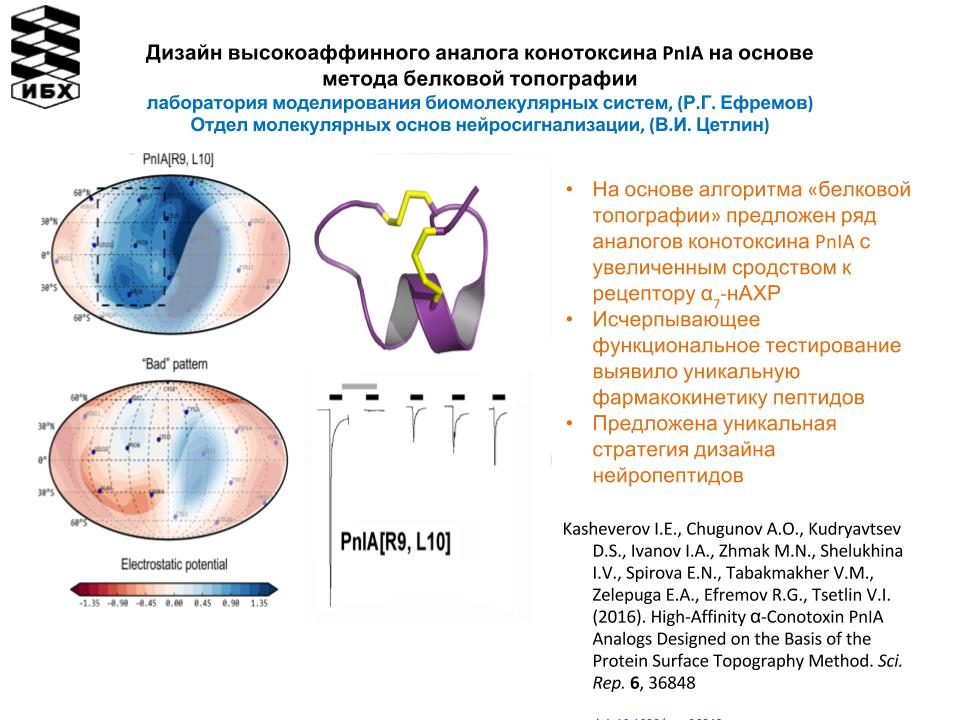
- Дизайн высокоаффинного аналога конотоксина PnlA на основе метода белковой топографии (Лаборатория моделирования биомолекулярных систем Р.Г. Ефремова, Отдел молекулярных основ нейросигнализации В.И. Цетлина).
- Конструирование соединений направленного действия для диагностики и терапии социально-значимых заболеваний и разработка фундаментальных принципов конструирования мультифункциональных соединений направленного действия для диагностики и терапии социально-значимых заболеваний (Лаборатория молекулярной иммунологии С.М. Деева и Лаборатория полимеров для биологии В.П. Зубова).
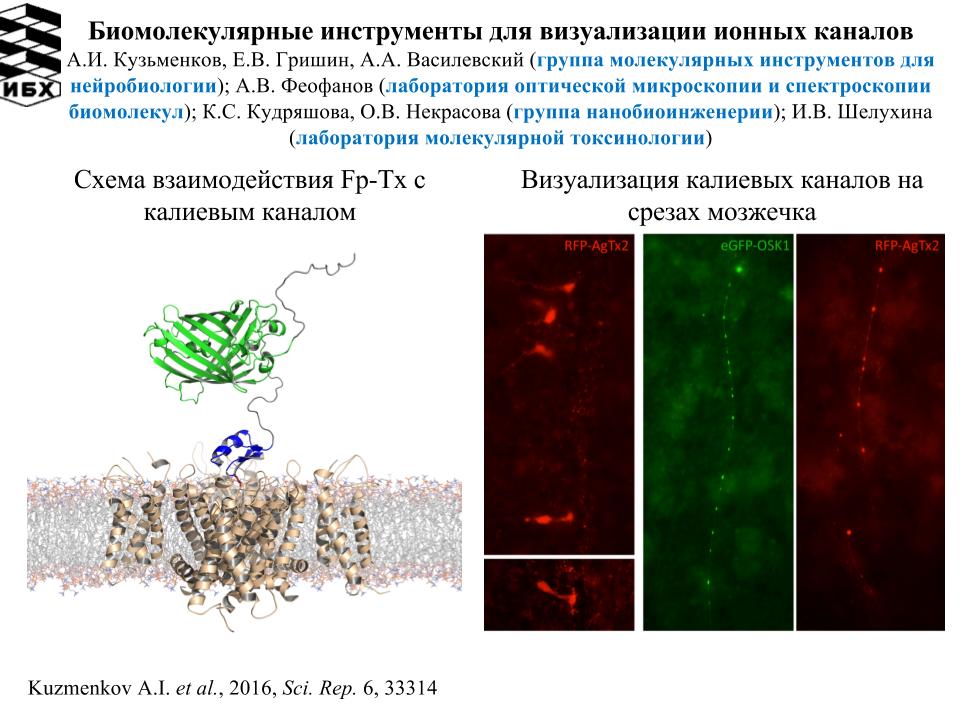
- Новые технологии активации и визуализации молекулярных объектов и событий в нервной системе: термооптогенетические технологии стимуляции нервной системы, сопряженные с визуализацией молекулярных событий in vivo и биомолекулярные инструменты для визуализации ионных каналов (Лаборатория молекулярных технологий В.В. Белоусова, Лаборатория геномики адаптивного иммунитета Д.М. Чудакова, Группа молекулярных инструментов для нейробиологии В.А. Василевского, Лаборатория оптической микроскопии и спектроскопии биомолекул А.В. Феофанова, Группа нанобиоинженерии О.В. Некрасовой и Лаборатория молекулярной токсинологии Ю.Н. Уткина).
- Глубокий структурно-функциональный анализ влияния аминокислотных замен на фотофизические свойства зеленых флуоресцентных белков (Лаборатория биофотоники К.А. Лукьянова, Лаборатория геномики адаптивного иммунитета Д.М. Чудакова, Группа синтеза природных соединений И.В. Ямпольского, Лаборатория сравнительной и функциональной геномики Ю.Б. Лебедева).
- Новый механизм биолюминесценции высших грибов и стереоселективный синтез углеродного скелета паналя – терпеноида из биолюминесцентных грибов Panellus stipticus (Группа синтеза природных соединений И.В. Ямпольского).
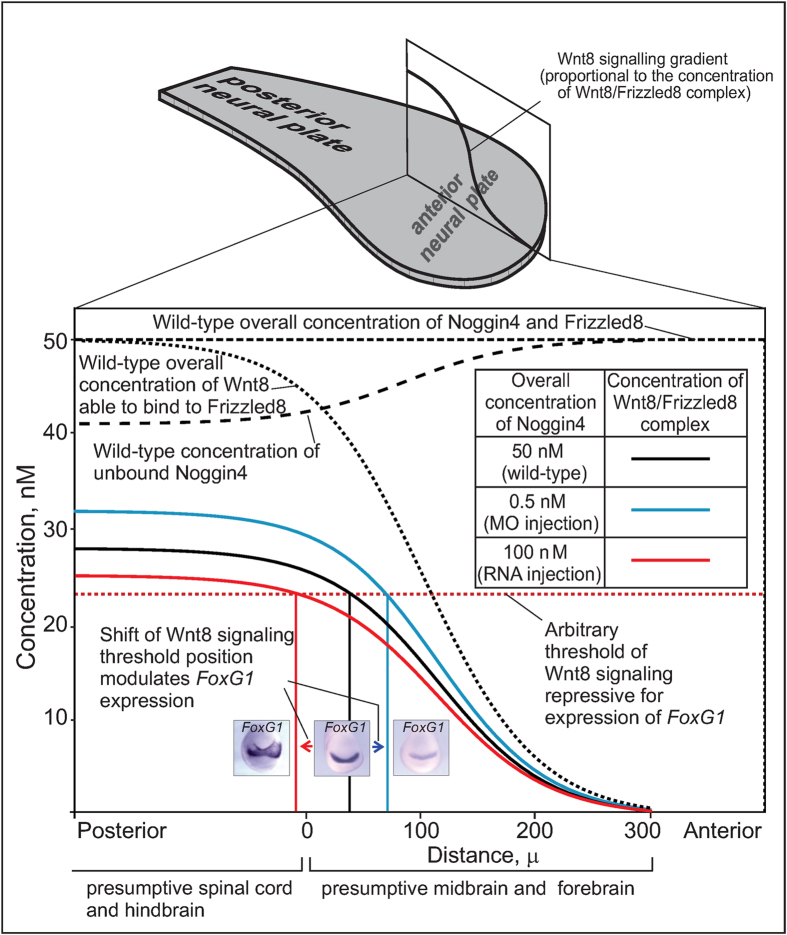
- Секретируемый белок Noggin4 – дальнодействующий ингибитор Wnt8 (Лаборатория молекулярных основ эмбриогенеза А.Г. Зарайского, Лаборатория биофотоники К.А. Лукьянова, Лаборатория биокатализа А.Г. Габибова). Во время формирования нервной системы у эмбрионов каскад Wnt8 распространяется от задних областей нервной системы к передним и образует градиент сигнализации Wnt8, который отвечает за эмбриональные процессы (на картинке изображён в виде линии).
- Концепция виртуального созревания антител на основе QM/MM расчетов реакций деградации антигенов (Группа комбинаторных методов конструирования биокатализаторов И.В. Смирнова, Лаборатория биокатализа А.Г. Габибова).
- Структурная реорганизации нуклеосом под действием белкового фактора FACT (Лаборатория оптической микроскопии и спектроскопии биомолекул А.В. Феофанова, Отдел биоинженерии М.П. Кирпичникова).
- Метод массированного безошибочного анализа репертуаров полноразмерных вариабельных участков генов иммуноглобулинов (Лаборатория геномики адаптивного иммунитета Д.М. Чудакова, Лаборатория сравнительной и функциональной геномики Ю.Б. Лебедева).
Достижения отделов ИБХ РАН
Отдел пептидно-белковых технологий (руководитель – В.Т. Иванов) в 2016 году продемонстрировал возможности современного обратно-пептидомного и протеомного подходов, объединения в одной работе биоинформатических и экспериментальных данных, позволивших выдвинуть новую гипотезу о механизме развития синдрома Гийена-Барре (Лаборатория химии пептидов В.Т. Иванова, Лаборатория протеомики В.М. Говоруна). Отдел впервые предложил применить алгоритмы для виртуального отбора наиболее эффективных иммуноглобулинов, обладающих каталитической активностью, провел вторую фазу клинических испытаний препарата Xemys для лечения рассеянного склероза (Лаборатория биокатализа А.Г. Габибова), предложил механизм роста разветвленных наноуглеродных структур на острие зонда атомно-силового микроскопа, методом осаждения из газовой фазы, стимулированного плазмой, получил сверхострые зонды для атомно-силового микроскопа, позволяющие получить высокое разрешение при исследовании в атомно-силовом микроскопе (Лаборатория протеомики В.М. Говоруна), а также определил пространственную структуру фотопереключаемого флуоресцентного белка wt DendFP (коралл Dendronephthya sp.) в зеленой и фотоконвертированной красной формах при разрешении 1.81A и 2.14A, соответственно и установил пространственную организацию и структурно-функциональную взаимосвязь новых флуоресцентных белков с хромофором на основе триптофана (Лаборатория рентгеноструктурного анализа В.З. Плетнева, Группа химии хромопротеинов В.И. Мартынова).

Отдел иммунологии (руководитель – Р.В. Петров) показал, что на ранних стадиях формирования аллергии возможно прямое переключение В-клеток на синтез IgE антител и в мышиной модели аллергического воспаления дыхательных путей продемонстрирован анти-воспалительный эффект экзогенных HSP70, свидетельствующий о комплексном иммунорегуляторном действии этих протеинов (Лаборатория клеточных взаимодействий А.М. Сапожникова). Сотрудники Отдела (Лаборатория молекулярной иммунологии С.М. Деева) впервые разработали для глубокой фотодинамической терапии системы внутритканевого возбуждения фотосенсибилизаторов, в том числе с помощью антистоксовых нанофосфоров и рибофлавина, вызывающих стойкую регрессию опухоли при облучении ближним инфракрасным светом. По мнению исследователей, это позволит решить проблемы доставки света вглубь тканей и расширит возможности фотодинамической терапии опухолей глубинных тканей и метастазов.
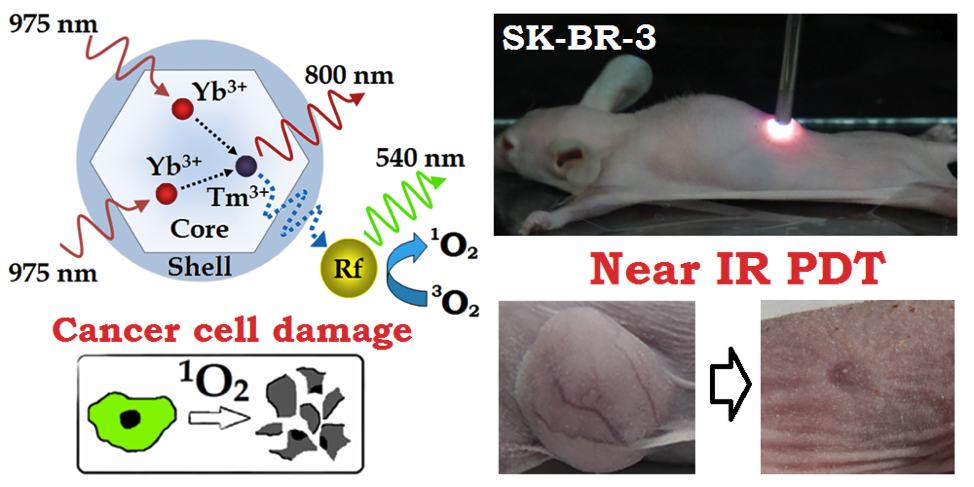
Нанокомплекс состоит из апконвертирующей наночастицы и молекулы витамина B2 (Rf) для глубокой фотодинамической терапии и диагностики злокачественных опухолей. Источник: Евгений Хайдуков.
Отдел структурной биологии (руководитель – А.С. Арсеньев) с помощью ЯМР-спектроскопии высокого разрешения показал, что смена мембранно-подобного окружения приводит к альтернативной димеризации трансмембранного домена EGFR (рецептор EGFR играет ведущую роль в процессах пролиферации и дифференциации клеток в норме и при патологиях организма человека) и предложил новый механизм аллостерической передачи сигнала РТК через мембрану клетки посредством согласованных белок-липидного и белок-белковых взаимодействий, объясняющий ряд парадоксов, наблюдаемых при активации EGFR и других РТК (Лаборатория биомолекулярной ЯМР-спектроскопии А.С. Арсеньева). Исследователи впервые in silico изучили температурную активацию рецептора TRPV1, что в дальнейшем можем помочь при создании селективных лигандов TRPV1 для разработки анальгетических лекарств, а также разработали дизайн высокоаффинного аналога конотоксина PnlA на основе метода белковой топографии (Лаборатория моделирования биомолекулярных систем Р.Г. Ефремова). Сотрудникам Отдела удалось разработать методики флуоресцентной микроскопии одиночных нуклеосом и их комплексов, а также установить, что белковый фактор FACT раскручивает нуклеосомную ДНК обратимо, независимо от АФТ, симметрично и без потери гистонов (Лаборатория оптической микроскопии и спектроскопии биомолекул А.В. Феофанова).
Отдел геномики и постгеномных технологий (руководитель – С.А. Лукьянов) работал по ряду направлений. Во-первых, сотрудникам удалось определить значимость метилирования LINE-1 ретротранспозонов в циркДНК крови для диагностики рака легкого путем выделения гиперметилированных фрагментов с помощью ДНК-метил-связывающего белка (Methylated CpG Island Recovery Assay, MIRA) в комбинации с количественной ПЦР (Лаборатория структуры и функций генов человека Е.Д. Свердлова). Во-вторых, в рамках проекта ИБХ РАН и ФНКЦ ДГОИ им. Дмитрия Рогачева была отслежена динамика восстановления системы Т-клеточного иммунитета человека после терапевтической трансплантации гемопоэтических стволовых клеток (ТГСК, перспективный способ лечения онкологических заболеваний крови). В работе была изучена годовая динамика клонального состава периферических Т-лимфоцитов у пациентов с острыми детскими лейкозами, перенесшими терапевтическую ТГСК (Лаборатория геномики адаптивного иммунитета Д.М. Чудакова и Лаборатория сравнительной и функциональной геномики Ю.Б. Лебедева). В-третьих, исследователи разработали метод подготовки, секвенирования и анализа молекулярно баркодированных кДНК библиотек, впервые позволивший проводить безошибочный анализ полноразмерных вариабельных участков генов иммуноглобулинов (Лаборатория геномики адаптивного иммунитета Д.М. Чудакова). В-четвертых, сотрудники Отдела провели глубокий структурно-функциональный анализ влияния аминокислотных замен на фотофизические свойства зеленых флуоресцентных белков, результаты которого были опубликованы в журнале Nature (Лаборатория биофотоники К.А. Лукьянова, Лаборатория геномики адаптивного иммунитета Д.М. Чудакова, Группа синтеза природных соединений И.В. Ямпольского, Лаборатория сравнительной и функциональной геномики Ю.Б. Лебедева). В-пятых, исследователи на молекулярном уровне определили различия между детской и взрослой формами острого миелобластного лейкоза и острого лимфобластного лейкоза (Группа геномного анализа сигнальных систем клетки А.А. Буздина). Наконец, была разработана комплексная технологий стимуляции нейронов с помощью встроенных в них термочувствительных каналов ямкоголовых змей, являющейся альтернативой оптогенетики, так как основана на использовании инфракрасного светового диапазона, исключающего фотодинамическое повреждение ткани, система была протестирована на нейронах рыбы Danio rerio in vivo (Лаборатория молекулярных технологий В.В. Белоусова).
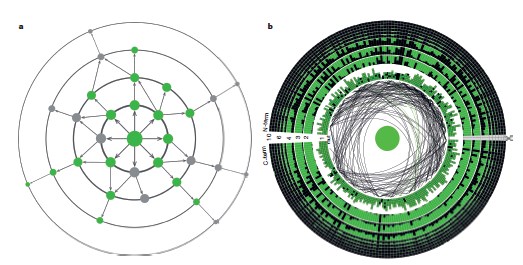
а. Иллюстрация концепции ландшафта приспособленности зеленого флуоресцентного белка. Зеленая точка в центре - немутированный белок, точки на окружностях - мутантные варианты с одной, двумя и тремя отличающимися аминокислотами. Цвет отражает фенотип (индивидуальные свойства) мутанта: зеленый - мутант ярко светится, серый - мутант не светится. Стрелки отражают возможные маршруты движения по ландшафту приспособленности. b. Визуализация всех полученных в работе данных на одной картинке. Последовательность зеленого флуоресцентного белка изображена в виде окружности: каждый маленький сектор обозначает одну аминокислотную позицию. Чем дальше круг находится от центра, тем больше мутаций содержит белок. Доля зеленого в каждом секторе отражает долю функциональных мутантов.
Отдел молекулярной нейробиологии (руководитель – С.К. Завриев) создал высокоаффинные химерные молекулы FP-Tx на основе флуоресцентных белков (FP) и токсинов скорпионов (Tx), селективно воздействующих на потенциал-чувствительные калиевые каналы человека, которые можно использовать для визуализации ионных каналов, скрининговых технологий и диагностики ряда заболеваний (Группа молекулярных инструментов для нейробиологии А.А. Василевского, Лаборатория оптической микроскопии и спектроскопии биомолекул А.В. Феофанова, Группа нанобиоинженерии О.В. Некрасовой, Лаборатория молекулярной токсинологии Ю.Н. Уткина). Также исследователи определили структуру элиситорного (в данном случае – стимулирующего защитную реакцию растений томата) белка CS20EP из штамма CS-20 гриба Fusarium oxysporum (Лаборатория молекулярной диагностики С.К. Завриева).
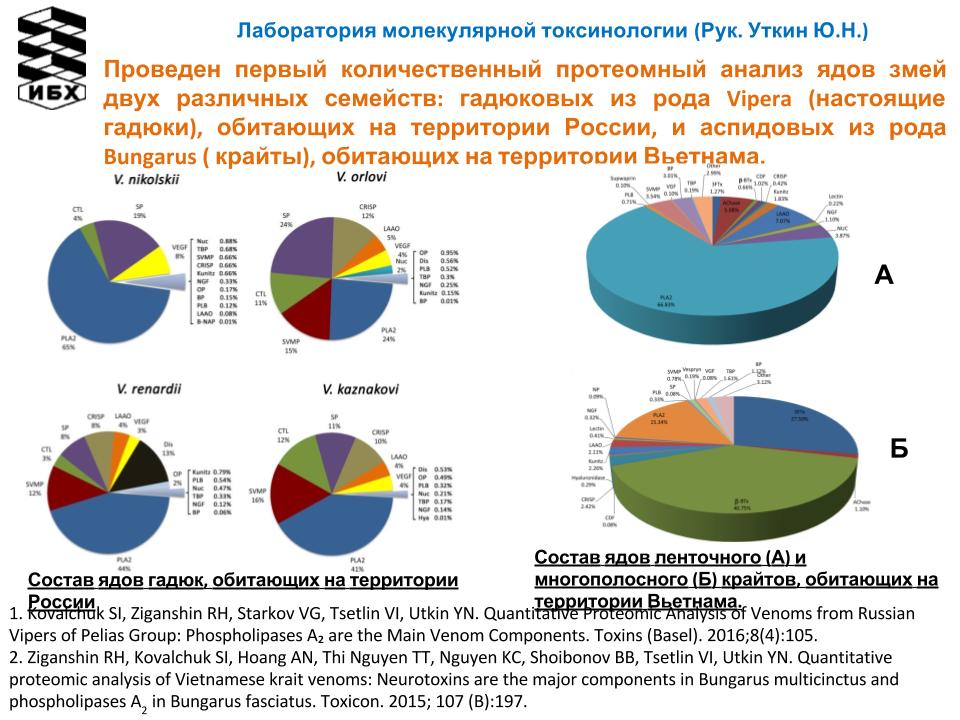
Отдел молекулярных основ нейросигнализации (руководитель – В.И. Цетлин) на основе метода топографии белковых поверхностей, предложенного в ИБХ РАН, сконструировал и синтезировал аналоги a-конотоксина PnIA, значительно превосходящие природное соединение по сродству к нейрональному a7 никотиновому рецептору. Методом поверхностного плазмонного резонанса показана способность ws-Lynx1 (водорастворимой модели Lynx1, эндогенного мембрано-связанного белка) связываться, как с ацетилхолин-связывающим белком, так и с полноразмерным прокариотическим рецептором GLIC. Сотрудники провели первый количественный протеомный анализ ядов змей двух различных семейств: гадюковых из рода Vipera (настоящие гадюки), обитающих на территории России, и аспидовых из рода Bungarus (крайты), обитающих на территории Вьетнама (Лаборатория молекулярной токсинологии Ю.Н. Уткина). Кроме того, исследователями Отдела было установлено, что соединение из морской губки – ризохалин – с высокой эффективностью in vitro и in vivo подавляет жизнеспособность клеток рака простаты (Лаборатория лиганд-рецепторных взаимодействий И.Е. Кашеверова).
Отдел биоинженерии (руководитель – М.П. Кирпичников) предложил новый подход к исследованию молекулярных основ взаимодействия пептидных блокаторов с калиевым каналом Kv1.6, а также изучили трехпетельные белки семейства Ly6/uPAR – регуляторов важных процессов жизнедеятельности человека. Ими было показано, что белок Lynx-1 конкурирует с β-амилоидным пептидом за связывание с nAChR, а SLURP-2 является универсальным регулятором гомеостаза кератиноцитов.

Отдел «Учебно-научный центр» (руководитель – Т.В. Овчинникова) обнаружил и изучил новые липид-транспортирующие белки (LTP) в листьях и стеблях укропа Anethum graveolens L., в семенах гороха Pisum sativum L. и чечевицы Lens culinaris L. Установлена структура белка LTP укропа Ag-LTP, обладающего противогрибковой активностью. В семенах гороха обнаружено подсемейство из трёх белков Ps-LTP1-3. Выделен индивидуальный природный Ps-LTP1 и получен его рекомбинантный аналог. Показано, что Ps-LTP1 является пищевым аллергеном гороха. Новый пищевой аллерген внесён в международную базу данных WHO/IUIS под аббревиатурой Pis s 3. Получены рекомбинантные аналоги белка укропа Ag-LTP и изоформ аллергена чечевицы Len c 3 – Lc-LTP1 и Lc-LTP3.
Достижения лабораторий ИБХ РАН
Лаборатория полимеров для биологии (руководитель – В.П. Зубов) получила биосовместимые полимерно-капсулированные реагенты на основе наночастиц с антистоксовой фотолюминесценцией.
Лаборатория биотехнологии (руководитель – А.И. Мирошников) получила рекомбинантные аналоги природных ингибиторов тромбина из различных кровососущих организмов
Лаборатория структурной биохимии (руководитель – О.В. Зацепина) продолжает изучать вопросы, связанные с выяснением роли ядрышек в образовании рибосом и участии в других жизненно-важных процессах, включая регуляцию клеточного цикла и пролиферации, уделив внимание вопросу локализации РНК и белков в предшественниках ядрышек ранних эмбрионов мышей.
Лаборатория молекулярных основ эмбриогенеза (руководитель – А.Г. Зарайский) установила, что секретируемый белок Noggin4 является дальнодействующим ингибитором Wnt8.
Лаборатория механизмов генной экспрессии (руководитель – Г.В. Шпаковский) обнаружила новые аналоги G-clamp с C8-линкерными группами в феноксазиновом кольце и применила их в детекции с помощью кПЦР низкокопийной дцРНК вируса Кемерово.
Лаборатория органического синтеза (руководитель – А.А. Формановский) совместно с Группой биоконъюгации (руководитель – В.А. Коршун) разработала метод дериватизации низкомолекулярных аминов для высокочувствительного определения с помощью высокоэффективной жидкостной хроматомасс-спектрометрии.
Лаборатория молекулярной биофизики (руководитель – В.А. Олейников) создала гибридный наноматериал с эффектом памяти – серебряная наночастица бактериородопсин (AgНЧ/БР).
Лаборатория синтетических вакцин (руководитель – О.М. Вольпина) выявила повышенный уровень природных антител к фрагменту рецептора нейротрофинов Р75 в сыворотках пациентов с мягкими когнитивными нарушениями.
Достижения групп ИБХ РАН
Группа синтеза природных соединений (руководитель – И.В. Ямпольский) впервые определила структуру оксилюциферина высших грибов, предложила уникальный механизм биолюминисценции и получила ряд аналогов люциферина грибов, обладающих отличающимся спектром биолюминесценции, а также осуществила полный синтез терпенового ядра паналя – активного компонента биолюминесцентных грибов Panellus stipticus.

Достижения подразделений филиала ИБХ РАН в г. Пущино
Лаборатория биологических испытаний (руководитель – А.Н. Мурашев) получила свидетельство о международном признании соответствия принципам надлежащей лабораторной практики (GLP) при выполнении неклинических исследований.
Лаборатория биотехнологии растений (руководитель – Я.И. Бурьянов) проанализировала метилирование промотора 35S в трансгенных растениях каланхоэ, экспрессирующих ген антимикробного пептида цекропина Р1. Данная работа показывает, что с помощью специфических условий культивирования растений можно регулировать синтез трансгенных антимикробных пептидов.
Лаборатория пептидных биорегуляторов (руководитель – Е.В. Наволоцкая) синтезировала пептиды октарфин (TPLVTLFK) и его цилический аналог cyclo (TPLVTLFK), повышающие устойчивость миокарда к стрессорным воздействиям и функциональным перегрузкам.
Группа молекулярной экологии (руководитель – О.Е. Трубецкая) обнаружила свободные аминокислоты в составе фракции гуминовых веществ с номинальной молекулярной массой более 150 кДа, что стало первым экспериментальным подтверждением существования супрамолекулярного гуминового комплекса.
Анализ публикационной активности ИБХ РАН
За 2016 год сотрудниками ИБХ РАН было опубликовано 410 статей (в 2015 году – чуть более 300 публикаций), из них – 250 в иностранных журналах и 160 русских журналах. Также было посчитано количество статей сотрудников ИБХ РАН в журналах с импакт-фактором выше 9. Если в 2015 году в таких журналах было опубликовано 7 статей с суммарным импакт-фактором 101,456, то в 2016 году показатели возросли и достигли 15 статей суммарным импакт-фактором 303,97.
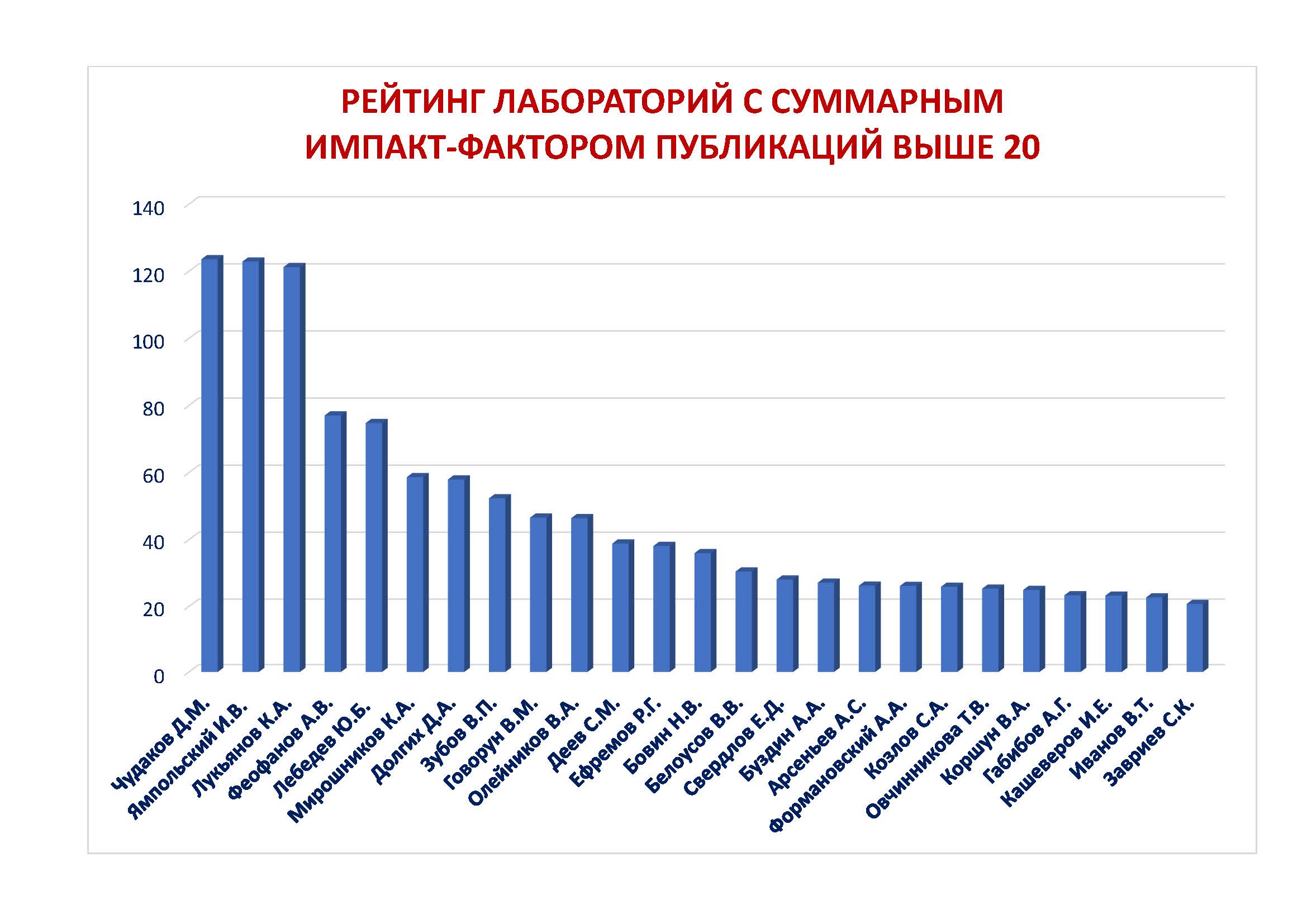
Исходя из суммарного и индивидуального импакт-фактора публикаций ИБХ РАН в рейтинговых журналах, лидирующие позиции занял Отдел геномных и постгеномных технологий (246,788), Отдел структурной биологии (132,306) и Отдел пептидно-белковых технологий (105,105). Следом за ними в рейтинге идет Отдел биоинженерии (58,568), Отдел иммунологии (58,338), Отдел молекулярной нейробиологии (47,986), Отдел молекулярных основ нейросигнализации (40,163), Отдел «Учебно-научный центр» (25,368) и Отдел «Научно-инновационный центр Технопарк» (13,14). В рейтинге лабораторий с суммарным импакт-фактором публикаций выше 20 первые строчки занимает Лаборатория геномики адаптивного иммунитета, Группа синтеза природных соединений и Лаборатория биофотоники.
С более подробной статистикой можно познакомиться с помощью презентации, прикрепленной к тексту.
28 января 2017 года

